
����Ŀ��ijͬѧ������������ȡ������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3 �� �������������ʣ���ȡ��ˮ������������FeSO47H2O�����������ͼ���̣�����˵������ȷ���ǣ������� 
A.�ܽ�����ѡ���������ᣬ�Լ�Xѡ������
B.����1��һ������SiO2 �� ����pHΪʹAl3+ת��ΪAl��OH��3 �� �������2
C.����Һ2�õ�FeSO47H2O��Ʒ�Ĺ����У������������ֹ������
D.���ı䷽��������Һ1��ֱ�Ӽ�NaOH���������õ��ij����������ܽ⣬����Һ���ᾧ����Ҳ�ɵõ�FeSO47H2O
���𰸡�D
���������⣺��������ȡ������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3���������������ʣ���������м����������ᣬFe2O3��Al2O3���ᷴӦ���ɵ������������������������費��Ӧ�����ˣ�����1Ϊ�������裻����Һ�м������۽������ӻ�ԭΪ�������ӣ�����pHֵʹ��������ȫ���������������������ˣ�����2Ϊ������������Һ2Ϊ��������������Ũ������ȴ�ᾧ�����ˣ��õ������������壬
A�������̷�����֪���ܽ�����ѡ���������ᣬXΪ���ۣ���A��ȷ��
B�������̷�����֪������1��һ������SiO2������pHֵʹ��������ȫ�����������������������2Ϊ������������B��ȷ��
C�����������ױ������е���������������������ʧȥ�ᾧˮ�����Դ���Һ2�õ�FeSO47H2O��Ʒ�Ĺ����У������������ֹ�������ͷֽ⣬��C��ȷ��
D������Һ1�к��������Ӻ������ӣ��ӹ������������ƣ�������ת��Ϊƫ��������ӣ������������������ӽ���������������������������յõ�����������������������������D����
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ����С���ͬѧ�ھ�ȷ����Na2SO3��Һ��pHʱ������������Ϊ�ˣ����ǽ������侲��˼����������������ʵ�飬�ҿ����أ������˽���������뽻�����ۣ�
[��������]�ٳ�����0.1molL��1��H2SO3��Һ��pHԼΪ2.1��
��ͨ������£�H2SΪ��ɫ���и�����ζ�����壬��ˮ��Һ��Ϊ�����ᣮ������0.1molL��1��H2S��Һ��pHԼΪ4.5��
[ʵ�����]��ȷ��ȡ������Na2SO37H2O����25.20g�����1Lˮ��Һ�������pH=7.8��
���������ٴ�ȷ��ȡ25.20g�������壬�̶�����������600�����ϸ�����ǿ�������أ�ֻ����Ԫ�صĻ��ϼ۱仯����ۺ���ͼۣ�������Ϊ12.60g��
�۽�������֮12.60g�������Ԫ�ض��Զ��������������Na2SO3���죮��������ˮ��250mL��Һ�����pH=10.3��
[��������]Na2SO37H2O��ǿ���£�ʧȥ�ᾧˮ�����������˷ֽⷴӦ������������ԭ��Ӧ��
[��������]
��1��ʵ��������г��������ƾ��ơ����Ǽܼ������������豸�⣬����Ҫ�������� ��
��2����Na2SO37H2O����ʱҪ�������������Լ�Ҫ�����ֺͻ�ѧ����ʽ����˵���� ��
��3������Na2SO3�ڸ���ǿ���·����ֽⷴӦ�Ļ�ѧ����ʽ�� ��
��4��ʵ��ٺ͢��У����β�õ���ҺpH������ԣ�������Ľ����� �� ʵ�������Һ��pH=10.3��ԭ���ǣ�����ص����ӷ���ʽ��ʾ�� ��
��5��������Ƽ�ʵ�鷽�������������������뼰��������֤���������ʵ�鲽�衢����ͽ��ۣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ե����ʵ�����ϵ�NaHCO3��KHCO3�Ļ����a g��100 mL���ᷴӦ���������漰����������Ա�״���ƣ����ʱ�����ô���ĸ����ѧʽ��ʾ�����ػ���
��1���û������NaHCO3��KHCO3��������Ϊ ��
��2�������Ӧ�����������Ҫ��������CO2�����������֪�� �� ������ ��
��3�����û����������ǡ����ȫ��Ӧ������������ʵ���Ũ��Ϊ
��4����NaHCO3��KHCO3�����Ե����ʵ�����ϣ���a g����������������������ȫ��Ӧʱ������CO2�������V����ȡֵ��Χ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ȷ���ǣ� ��
A.�Ȼ�����Һ�м��������ˮ��Ӧ��ʵ����Al3++3NH3?H2O�TAl��OH��3��+3NH ![]()
B.��������ˮ�е��ؽ������ӣ�����Ͷ�������ȵ���ʵķ������д���
C.þ���Ͻ�ȿ���ȫ���ڹ��������ֿ���ȫ���ڹ���NaOH��Һ
D.�������ȷ�Ӧԭ�����ܷ�����Ӧ2Al+3MgO ![]() 3Mg+Al2O3
3Mg+Al2O3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ�У����ձ���ʢ��100mL 0.50molL��1 AgNO3��Һ�����ձ���ʢ��100mL 0.25molL��1CuCl2��Һ��A��B��C��D��Ϊ������ͬ��ʯī�缫��������һ��ʱ�����A����C����1.9g���� 
��1����ԴEΪ����FΪ����
��2��A���ĵ缫��ӦʽΪ �� ��������mol��
��3��B���ĵ缫��ӦʽΪ �� ��������mL���꣩��
��4��C���ĵ缫��ӦʽΪ �� ����������mol��
��5��D���ĵ缫��ӦʽΪ �� ��������mL���������
��6�����ձ��е���ʯ����Һ����������죬���������룬�ڼ��ձ������յõ���Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijϡ��Һ�к���Fe��NO3��3��Cu��NO3��2��HNO3 �� �������������ۣ���Һ��Fe2+��Ũ����������۵����ʵ���֮��Ĺ�ϵ��ͼ��ʾ������Һ��Fe��NO3��3��Cu�� NO3��2��HN03���ʵ���Ũ��֮��Ϊ�������� 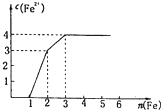
A.1��1��1
B.1��3��1
C.2��1��4
D.1��1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E����ԭ���������������Ԫ�أ�ԭ��������С��30����A�Ļ�̬ԭ��2p�����3��δ�ɶԵ��ӣ�C�Ļ�̬ԭ��2p�����1��δ�ɶԵ��ӣ�Eԭ���������1��δ�ɶԵ��ӣ���������3��ԭ�ӹ���Ҿ��������ӣ���D��Eͬ���ڣ��۵�����Ϊ2����
��1��д����̬Eԭ�ӵĵ����Ų�ʽ ��
��2��1mol A�ĵ��ʷ����Цм��ĸ���Ϊ ��
��3��A��B��C ����Ԫ�ص��⻯���ȶ�����ǿ������˳��Ϊ���û�ѧʽ��ʾ����
��4��A�ļ��⻯����ӵĿռ乹��Ϊ �� ����Aԭ�ӵ��ӻ������� ��
��5��C��D�γɵĻ�����ľ����ṹ��ͼ����֪�����߳�a cm�������ӵ�����ΪNA �� ������ܶ�Ϊ��=g/cm3 �� ���ú�a��NA�ļ���ʽ��ʾ�� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���ָ��ԭ��������Ԫ�أ������γ�AB2�����ӻ�������ǣ� ��
A. 6��8B. 12��9C. 12��17D. 20��17
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ŷ�����о�������1995��9��~10�¼����Ƴ������ϵ�һ����ԭ��������9������ԭ�ӣ��ҿ���������ȡ�����÷����ʵ���ƪ�¡������й��ڷ���ԭ��˵����ȷ����( )
A.������8������������ӣ�������8��������ĵ���
B.������8��������ĵ��ӣ�������8�������������
C.������8������������ӣ�������8�������������
D.������8������������ӣ�������8��������ĵ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com