
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物.试回答下列问题: 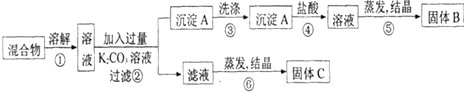
(1)B物质的化学式为 .
(2)该方案的明显失误是因某一步设计不当而使分离产物不纯,该步骤是(填序号)如何改进 .
(3)写出K2CO3的电离方程式 .
(4)写出 ②④两步中对应的离子方程式:
②
④ .
【答案】
(1)BaCl2
(2)⑥;应先在⑥步操作前的滤液中加足量盐酸后,蒸发结晶
(3)K2CO3═2K++CO32﹣
(4)Ba2++CO32﹣═BaCO3↓;BaCO3+2H+═Ba2++CO2↑+H2O
【解析】解:分离KCl和BaCl2两种固体混合物,可先溶于水,然后加入过量K2CO3使BaCl2转化为A碳酸钡沉淀,过滤后沉淀加入盐酸可生成BaCl2溶液,经⑤蒸发、结晶后可得B固体BaCl2 , 操作②所得滤液为KCl和K2CO3的混合物,应加入过量盐酸可得KCl,固体C为KCl;(1)氯化钾和氯化钡溶液中加入碳酸钾溶液可以生成碳酸钡沉淀,则沉淀A为BaCO3;过滤后碳酸钡沉淀中加入盐酸可生成BaCl2溶液,经⑤蒸发、结晶后可得B固体BaCl2 , 所以答案是:BaCl2;(2)蒸发结晶前应加入适量稀盐酸,将过量的碳酸钾转化成氯化钾,否则晶体不纯,所以答案是:⑥;应先在⑥步操作前的滤液中加足量盐酸后,蒸发结晶;(3)K2CO3为强电解质,完全电离,电离方程式为K2CO3═2K++CO32﹣ , 所以答案是:K2CO3═2K++CO32﹣;(4)②加入碳酸钾生成碳酸钡沉淀,反应的离子方程式为Ba2++CO32﹣═BaCO3↓,④为碳酸钡和盐酸的反应,离子方程式为BaCO3+2H+═Ba2++CO2↑+H2O,
所以答案是:Ba2++CO32﹣═BaCO3↓;BaCO3+2H+═Ba2++CO2↑+H2O.


科目:高中化学 来源: 题型:
【题目】对于物质的量浓度均为0.1 mol·L-1,体积相同的盐酸和醋酸两种溶液的说法正确的是
A.中和碱的能力相同B.水的电离程度相同
C.OH-的物质的量浓度相同D.H+的物质的量浓度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,ag气体A与bg气体B的分子数相等,則下列说法中不正确的是( )
A.A和B的相对分子质最之比为a:b
B.同温同压下,A和B的原子数之比为b:a
C.同质量的A和B的物质的量之比为b:a
D.同温同压下,同体积的A和B的质量之比为a:b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】端炔烃在催化剂存在下可发生偶联反应,称为Glaser反应。
![]()
该反应在研究新型发光材料、超分子化学等方面具有重要价值。如图是用利用Glaser反应制备化合物E的一种合成路线:

回答下列问题:
(1)B的化学名称为______________________________。
(2)③的反应类型为_________________________________。
(3)E的结构简式为__________________________________________________。用1 mol E合成1,4-二苯基丁烷,理论上需要消耗氢气________________________________mol。
(4)化合物(![]() )也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
)也可发生Glaser偶联反应生成聚合物,该聚合反应的化学方程式为____________________________________________________________________________________________________________。
(5)芳香化合物F是C的同分异构体,其分子中只有两种不同化学环境的氢,数目比为3:1,写出其中2种的结构简式_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应N2+3H2![]() 2NH3的能量变化如图所示,该反应的热化学方程式是( )
2NH3的能量变化如图所示,该反应的热化学方程式是( )

A. N2(g)+3H2(g) ![]() 2 NH3(l) ΔH=(b+c-a) kJ·mol-1
2 NH3(l) ΔH=(b+c-a) kJ·mol-1
B. N2(g)+3H2(g) ![]() 2NH3(g) ΔH=(a+b) kJ·mol-1
2NH3(g) ΔH=(a+b) kJ·mol-1
C. N2(g)+3H2(g) ![]() 2NH3(l) ΔH=2(a-b-c) kJ·mol-1
2NH3(l) ΔH=2(a-b-c) kJ·mol-1
D. N2(g)+3H2(g) ![]() 2NH3(g) ΔH=2(b-a) kJ·mol-1
2NH3(g) ΔH=2(b-a) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式或说法正确的是( )
A. 甲烷的燃烧热为ΔH=-890 kJ·mol-1 ,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890 kJ· mol-1
B. 500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1
C. 已知:H2(g)+F2(g)=2HF(g) ΔH=-270 kJ·mol-1 ,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ
D. 在C中相同条件下,2 mol HF气体的能量小于1 mol氢气与1 mol氟气的能量总和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体),下列分析或结果错误的是

A. 原混合酸中HNO3的物质的量为0.1 mol
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+ == 3Fe2+,BC段产生氢气
C. 第二份溶液中最终溶质为FeSO4
D. H2SO4浓度为2.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分离说法正确的是( )
A. 可用加热法分离氯化钠和碳酸钙
B. 蒸馏和蒸发都用来分离液体混合物
C. 工业上制无水酒精通常是将生石灰与95%酒精混合后蒸馏
D. 碘水中加四氯化碳振荡静置后,上层为紫色,下层几乎为无色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com