

 �����Ӳ�ṹ��ͬ�˵����Խ�����Ӱ뾶ԽС�����Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶��С�����˳��ΪNa+��O2-��Cl-��
�����Ӳ�ṹ��ͬ�˵����Խ�����Ӱ뾶ԽС�����Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶��С�����˳��ΪNa+��O2-��Cl-�� ��Na+��O2-��Cl-��
��Na+��O2-��Cl-��

 ��Уͨ��֤��Ч��ҵϵ�д�
��Уͨ��֤��Ч��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������ʹ��ˮ��ɫ SO2+Br2+2H2O=4H++SO42-+2Br- |
| B����ʳ����ϴ��ˮƿ���ڱڸ��ŵ�ˮ����CaCO3�� CO32-+2H+=CO2��+H2O |
| C������ͭ��Ba��OH��2��Һ��Ӧ Cu2++2OH-=Cu��OH��2�� |
| D������CO2ͨ��Na2SiO3��Һ��CO2+SiO32-+H2O=CO32-+H2SiO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ʾ���л��ﹲ�У�����������ṹ����������
��ʾ���л��ﹲ�У�����������ṹ����������| A��24�� | B��28�� |
| C��32�� | D��36�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������Ԫ��A��B��C��D�����ڱ��е�λ����ͼ1��ʾ��B��D����������֮��Ϊ12�����߿��γ�DB2��D
������Ԫ��A��B��C��D�����ڱ��е�λ����ͼ1��ʾ��B��D����������֮��Ϊ12�����߿��γ�DB2��D| B | 3 |
| H | 2 |
| ��ѧʽ | Ag2SO4 | AgBr |
| �ܽ�ȣ�g�� | 0.796 | 8.4��10-6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| Na | Mg | Si | |
| I1/kJ?mol-1 | 496 | 738 | 787 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | ���ձ��м�����Լ�����������mL�� | ���� | ��Һ��ʼ����ʱ�䣨min�� | ||||
| 0.1 mol?L-1 KI��Һ |
H2O | 0.01 mol?L-1 X ��Һ |
0.1 mol?L-1 ˫��ˮ |
1 mol?L-1 ϡ���� | |||
| 1 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | �� | 1.4 |
| 2 | 20.0 | m | 10.0 | 10.0 | n | �� | 2.8 |
| 3 | 10.0 | 20.0 | 10.0 | 20.0 | 20.0 | �� | 2.8 |
| 4 | 20.0 | 0 | 10.0 | 10.0 | 40.0 | �� | t |
| 5 | 20.0 | 10.0 | 10.0 | 20.0 | 20.0 | 5��Fe2��SO4��3 | 0.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
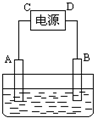 ��һ�����ξ��壬�仯ѧʽ��ʾΪM��NO3��x?nH2O���ⶨ��Ħ������Ϊ242g?mol-1��ȡ1.21g�þ�������ˮ���100mL��Һ��������Һ������ͼ��ʾװ���У���ʯī���缫���е�⣮����0.01mol����ͨ���缫ʱ����Һ�еĽ���������ȫ����������A���õ�����0.32g���ش�
��һ�����ξ��壬�仯ѧʽ��ʾΪM��NO3��x?nH2O���ⶨ��Ħ������Ϊ242g?mol-1��ȡ1.21g�þ�������ˮ���100mL��Һ��������Һ������ͼ��ʾװ���У���ʯī���缫���е�⣮����0.01mol����ͨ���缫ʱ����Һ�еĽ���������ȫ����������A���õ�����0.32g���ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������¶� |
| B������ѹǿ |
| C������H2��Ũ�� |
| D��ʹ�ô��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com