
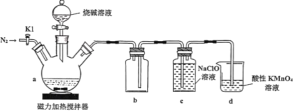
【题目】次磷酸钠(NaH2PO2)是有机合成的常用还原剂,一般制备方法是将黄磷(P4)和过量烧碱溶液混合、加热,生成次磷酸钠和PH3,PH3是一种无色、有毒且能自燃的气体。实验装置如图所示:
回答下列问题:
(1)在a中加入黄磷、活性炭粉末,打开K1,通入N2一段时间,关闭K1,打开磁力加热搅拌器,滴加烧碱溶液。
①仪器a的名称是______,已知NaH2PO2能与盐酸反应但不能与NaOH溶液反应,则次磷酸(H3PO2)是_______元弱酸。
②反应开始时,首先打开K1,通入N2一段时间,其目的是________。
③为了尽可能避免PH3造成的空气污染,拆卸装置前还要进行的一项操作是_________,a中反应的化学方程式为_______。
(2)装置c中生成NaH2PO2和NaCl,相关物质溶解度(S)如下,通过______的方法可分离出NaH2PO2固体。

(3)产品纯度测定:
取产品m g配成250mL溶液,取25mL于锥形瓶中,然后用0.01 mol/L KMnO4标准溶液滴定至终点(氧化产物是PO43-),达到滴定终点时消耗V1 mL KMnO4标准溶液,产品纯度为________。
【答案】三颈烧瓶 一 排尽装置中的空气,防止反应生成的PH3自燃引起爆炸 打开K1,继续通入一段时间N2 P4+3NaOH+3H2O![]() 3NaH2PO4+PH3↑ 蒸发浓缩、冷却结晶 ( 1.1 V1/m)%
3NaH2PO4+PH3↑ 蒸发浓缩、冷却结晶 ( 1.1 V1/m)%
【解析】
制备次磷酸钠,所用的药品是P4和NaOH溶液,加热条件下二者反应生成次磷酸钠的同时也生成了PH3,所以P4发生了歧化反应;题干中给出了关于PH3性质的信息,明确指出该物质无色,有毒能自燃,所以为了避免制备过程中生成的PH3发生自燃,需要在制备前,利用N2将装置内残余的空气排尽;此外,为了避免PH3造成的空气污染,也需要对装置a的出口气体进行吸收;因此,结合PH3还原性较强的特点,利用c中的NaClO对其进行氧化吸收,而装置d则起到验证是否吸收完全的作用,若未吸收完全,则也可对PH3进行吸收;至于装置b的作用,考虑到a装置出口气体组成中含有大量的易与NaClO反应的PH3,所以起到一定的防倒吸作用,防止c中的NaClO进入a中;制备反应结束后,由于装置内会残留部分PH3,出于安全性和环保性的考虑,需要在拆解装置前,持续通一段时间的N2,以尽可能地排尽装置内残余的PH3,使其在c和d装置中被吸收。
(1)①仪器a的名称为三颈烧瓶;由于次磷酸钠不能与NaOH溶液反应,所以![]() 不能电离出H+,所以次磷酸为一元弱酸;
不能电离出H+,所以次磷酸为一元弱酸;
②由于制备过程中会生成能自燃的PH3,所以需要在制备前通一段时间的N2,排尽装置内的空气,以防止PH3自燃;
③PH3有毒,制备结束后,装置内仍会残余少量的PH3气体,出于安全性和环保性的考虑,需要在拆解装置前,再持续通一段时间的N2,使残余的PH3尽可能地排尽,使其在c和d装置内被吸收;a中发生的是P4的歧化反应,制备出次磷酸钠的同时也产生了PH3,所以方程式为:![]() ;
;
(2)分析题中给出的不同温度下次磷酸钠和氯化钠溶解度的表格可知,次磷酸钠溶解度随温度变化很明显,所以从混合溶液中分离次磷酸钠的方法即:蒸发浓缩,冷却结晶;
(3)在计算产品纯度时,一定要注意题干中在用样品配制成溶液后,只取了一部分进行滴定;次磷酸钠与高锰酸钾反应,由题可知,P最终被氧化成![]() ,所以有:
,所以有:![]() ;所以产品纯度=
;所以产品纯度=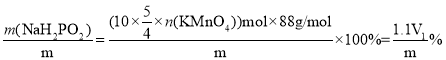 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[3,3]庚烷(![]() )是其中的一种。下列关于该化合物的说法不正确的是( )
)是其中的一种。下列关于该化合物的说法不正确的是( )
A. 与环庚烯互为同分异构体B. 二氯代物共有8种(不含立体异构)
C. 所有碳原子不可能处在同一平面D. 1mol该化合物含有18mol共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式不正确的是
A.NaHCO3在水中的电离方程式:NaHCO3 = Na++HCO![]()
B.氯化镁溶液与氨水反应的离子方程式:Mg2++2OH-= Mg(OH)2↓
C.Cl2与水反应的离子方程式:Cl2+H2O![]() H++Cl-+HClO
H++Cl-+HClO
D.醋酸钠水解的离子方程式CH3COO-+H2O![]() CH3COOH+OH-
CH3COOH+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所测的实验数据如图所示。
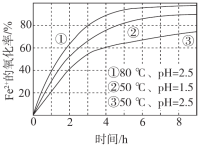
4Fe2+(aq)+4H+(aq)+O2(g)=4Fe3+(aq)+2H2O(l) ΔH>0
下列分析或推测合理的是
A.由①、②可知,pH越大,Fe2+越易被氧化
B.由②、③推测,若pH>7,Fe2+更难被氧化
C.pH=2.5、70℃时,0~3 h内Fe2+的平均消耗速率ν(Fe2+) < ![]() mol/(L·h)
mol/(L·h)
D.曲线②的变化趋势推测,反应吸热使得溶液温度下降,反应速率下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列对于Na2SO3与NaHSO3的混合溶液中微粒浓度关系的说法正确的是()
A.一定存在3c(Na+)=c(HSO3)+c(SO32)+c(H2SO3)
B.一定存在c(Na+)+c(H+)=c(HSO3)+c(SO32)+c(OH-)
C.若混合溶液中n(Na2SO3)=2n(NaHSO3)时,溶液呈碱性,则有c(Na+)>c(SO32)>c(HSO3)>c(OH)>c(H+)
D.若混合溶液中n(Na2SO3)=n(NaHSO3)时,溶液呈酸性,则有c(Na+)>c(HSO3)>c(H+)>c(SO32)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蕴藏在海底的大量“可燃冰”,其开发利用是当前解决能源危机的重要课题。CH4(g)+2H2O(g)![]() CO2(g)+4H2(g)ΔH3=+akJ·mol-1
CO2(g)+4H2(g)ΔH3=+akJ·mol-1
化学键 | C—H | H—H | H—O |
键能kJ/mol | b | c | d |
(1)写出甲烷的结构式___________
(2)C=O的键能为_______________kJ/mol(用含a、b、c、d的式子表示)
(3)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应。测得甲烷物质的量随时间变化如下表所示。0~10min内用H2O的浓度表示该反应的平均速率为υ(H2O)=_____________
时间/min | 0 | 10 | 20 | 40 | 50 | 60 |
n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 | 0.10 |
(4)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是_______________。
a.混合气体的平均相对分子质量保持不变b.CO2和H2的体积分数比为1﹕4
c.混合气体的密度保持不变d.1molCO2生成的同时有4molH-H键断裂
(5)写出甲烷燃料电池,以KOH溶液为介质时,负极的电极反应式______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在800 mL的大烧杯中放入碎纸屑把盛有50 mL 0.50 mol·L-1盐酸的100 mL烧杯放到大烧杯中,两只烧杯间填满碎纸屑。用泡沫塑料板做成大烧杯盖,通过盖子插入一根环形玻璃搅拌棒和一支温度计,测定溶液的温度。迅速往盐酸中加入 50 mL 0.55 mol·L-1NaOH溶液,盖好盖子,搅拌溶液,观察温度的变化。当温度保持稳定时,记录读数,取出装有反应液的烧杯,倒出溶液,清洗干净,保持内外杯壁干燥。重复进行三次实验。用这一实验可以粗略测定中和热。
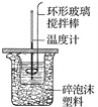
(1)烧杯间填满碎纸屑的作用是____________。
(2)要重复进行三次实验的目的是_____________。
(3)烧杯若不盖泡沫塑料板,求得的中和热数值将________(填“偏大”“偏小”或“无影响”)。
(4)实验中若改用60 mL 0.50 mol·L-1盐酸和50 mL 0.55 mol·L-1NaOH溶液进行上述反应,与上述实验相比,所放出的热量________(填“相等”或“不相等”),所求中和热________(填“相等”或“不相等”),理由是_______。
(5)三次实验测得的数据中,起始时盐酸与NaOH溶液温度相同,而终止温度与起始温度之差(t2-t1)分别为①2.3 ℃,②2.4 ℃,③2.5 ℃。则最终代入计算式的温度差的平均值为________℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主族。下列说法正确的是
A. 原子半径:r(W) > r(Z) > r(Y)
B. 由X、Y 组成的化合物中均不含共价键
C. Y 的最高价氧化物的水化物的碱性比Z的弱
D. X 的简单气态氢化物的热稳定性比W的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粮食仓储常用磷化铝(A1P)熏蒸杀虫,A1P遇水即产生强还原性的PH3气体。国家标准规定粮食中磷化物(以PH3计)的残留量不超过0.05 mgkg-1时为合格。某小组同学用图所示实验装置和原理测定某粮食样品中磷化物的残留量。C中加入100 g原粮,E 中加入20.00mL2.50×l0-4molL-1KMnO4溶液(H2SO4酸化),C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中的溶液。
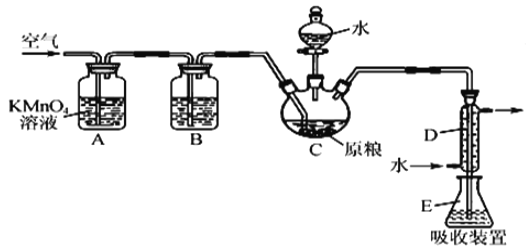
(1)装置A中的KMnO4溶液的作用是_____。
(2)装置B中盛装焦性没食子酸的碱性溶液吸收空气中的O2。若去掉该装置,则测得的磷化物的残留量______________________(填“偏髙”“偏低”或“不变”)。
(3)装置E中PH3氧化成磷酸,MnO4-被还原为Mn2+,写出该反应的离子方程式:___________
(4)收集装置E中的吸收液,加水稀释至250 mL,量取其中的25.00 mL于锥形瓶中, 用4.0×l0-5molL-1的Na2SO3标准溶液滴定,消耗Na2SO3标准溶液20.00mL,反应原理是 SO32-+MnO4-+H+→SO42-+Mn2++H20(未配平)通过计算判断该样品是否合格(写出计算过程)___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com