
| A. | 金属间发生置换反应 | |
| B. | 金属元素的最高价氧化物对应水化物的碱性强弱 | |
| C. | 1mol金属单质在反应中失去电子的多少 | |
| D. | 金属元素的单质与水或酸反应置换出氢气的难易 |
分析 A.活泼金属能将不活泼金属从其盐中置换出来;
B.金属元素的最高价氧化物对应的水化物的碱性越强,则失电子能力越强;
C.金属单质在反应中失去电子的能力越强则失电子的能力越强;
D.金属元素的单质与水或酸反应置换出氢气越容易,则失电子能力越强.
解答 解:A.活泼金属能将不活泼金属从其盐中置换出来,通过金属间发生的置换反应能用于判断金属性强弱,故A不选;
B.金属元素的最高价氧化物对应的水化物的碱性越强,则失电子能力越强,可以通过金属元素的最高价氧化物对应的水化物的碱性强弱判断金属性强弱,故B不选;
C.1mol金属单质失电子的多少由原子结构决定,与失电子能力强弱无关,所以1mol金属单质在反应中失去电子的多少不能用于判断金属性强弱,故C选;
D、金属元素的单质与水或酸反应置换出氢气越容易,则失电子能力越强,金属元素的单质与水或酸反应置换出氢气的难易程度可以判断金属性强弱,故D不选;
故选B.
点评 本题考查元素性质和元素周期表的递变规律,题目难度不大,明确元素周期律内容为解答关键,注意掌握判断金属性强弱的常用方法,C为易错点,注意金属性与得失电子数目无关.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
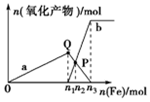 含1mol 溶质HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物与铁粉物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断正确的是( )
含1mol 溶质HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物与铁粉物质的量的关系如图所示(已知稀硝酸的还原产物只有NO).下列有关判断正确的是( )| A. | 曲线a表示Fe2+,曲线b表示Fe3+ | |
| B. | P点时总反应的离子方程式可表示为5Fe+16H++4NO3-═3Fe2++2Fe3++4NO↑+8H2O | |
| C. | n2=0.3 | |
| D. | n3:n1=3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
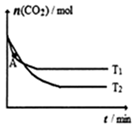 容积固定的密闭容器中,充入一定体积的CO2和H2,发生反应:CO2(g)+3H2(g)?CH3OH (g)+H2O(g).测得不同温度下CO2的物质的量随时间变化如图.下列说法正确的是( )
容积固定的密闭容器中,充入一定体积的CO2和H2,发生反应:CO2(g)+3H2(g)?CH3OH (g)+H2O(g).测得不同温度下CO2的物质的量随时间变化如图.下列说法正确的是( )| A. | 该反应为吸热反应 | |
| B. | T1、T2对应的平衡常数K1>K2 | |
| C. | T1时,图中A点的正反应速率小于逆反应速率 | |
| D. | T2时,若上述反应在压强恒定的密闭容器中进行,达平衡的时间变短 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2$→_{高温、高压、催化剂}^{H_{2}}$NH3$\stackrel{HCl(aq)}{→}$NH4Cl(aq) | |
| B. | AgNO3$\stackrel{NH_{3}•H_{2}O}{→}$[Ag(NH3)2]OH(aq)$→_{△}^{蔗糖}$ Ag | |
| C. | SiO2$\stackrel{HCl(aq)}{→}$SiCl4$→_{高温}^{H_{2}}$Si | |
| D. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$ Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | W(g) | X(g) | Y(g) | Z(g) |
| 初始浓度(mol/L) | 4.0 | 2.0 | 0 | 0 |
| 2min末浓度(mol/L) | 2.4 | 1.2 | 0.8 | 1.6 |
| A. | 2min内X的平均速率为0.6mol/(L•min) | |
| B. | 该反应的化学方程式可表示为:2W(g)+X(g)?2Y+Z | |
| C. | 若达到平衡后保持压强不变充入Ne,平衡不移动 | |
| D. | 平衡后再加入W,则W的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中性溶液:Cu2+、Fe3+、NO3-、I- | |
| B. | 加入硫氰化钾显血红色的溶液:K+、NH4+、Cl-、NO3- | |
| C. | 加入Al能放出大量H2的溶液中:NH4+、Fe2+、NO3-、SO42- | |
| D. | 常温下,c(H+)/c(OH-)=1×1012的溶液:K+、AlO2-、CO32-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
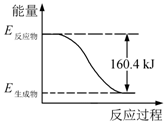 2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室.火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1mol气态水过程中的能量变化图.
2016年9月我国成功利用大功率运载火箭发射“天宫二号”空间实验室.火箭推进器中装有还原剂肼(N2H4)和强氧化剂过氧化氢(H2O2),如图是一定量肼完全燃烧生成氮气和1mol气态水过程中的能量变化图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个D216O分子所含的中子数为8 | |
| B. | NH4Cl是只含非金属元素的共价化合物 | |
| C. | HCl的电子式为 | |
| D. | H2S不如HF稳定性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 反应类型加聚反应
反应类型加聚反应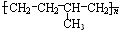 单体结构简式为CH2=CH2和CH3-CH=CH2.
单体结构简式为CH2=CH2和CH3-CH=CH2.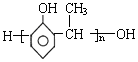 单体结构简式为
单体结构简式为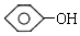 和CH3CHO.
和CH3CHO.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com