分析:A在氢氧化钠水溶液、加热条件下得到B、C,A中含有酯基,而B与足量二氧化碳反应得到H,H遇FeCl
3溶液显紫色,则H属于酚类,C能与银氨溶液反应,则C中应含有-CHO,C酸化后再与氢气发生加成反应得到D,则D中含有-COOH、-OH,D发生缩聚反应得到(C
4H
6O
2)
n,结合J中所有碳原子在一条直线上,可推知D为HOCH
2CH
2CH
2COOH,F能与溴发生反应得到G,G发生消去反应生成J,J分子中所有碳原子在一条直线上,则J存在-C≡C-三键,结合C的所有碳原子在同一平面上,可知C、E、F中含有C=C双键,综上分析,可推知C为OHC-CH=CH-COONa,顺推可得E为NH
4OOC-CH=CH-COONa,F为HOOC-CH=CH-COOH,G为HOOCCHBrCHBrCOOH,J为HOOC-C≡C-COOH.烃的含氧衍生物A的蒸气密度是相同条件下H
2的88倍,则其相对分子质量=88×2=176,结合C的结构可知H的相对分子质量=176+18-100=94,而H为酚类,可知H为
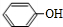
,B为苯酚钠,故A为
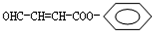
,据此解答.
解答:
解:A在氢氧化钠水溶液、加热条件下得到B、C,A中含有酯基,而B与足量二氧化碳反应得到H,H遇FeCl
3溶液显紫色,则H属于酚类,C能与银氨溶液反应,则C中应含有-CHO,C酸化后再与氢气发生加成反应得到D,则D中含有-COOH、-OH,D发生缩聚反应得到(C
4H
6O
2)
n,结合J中所有碳原子在一条直线上,可推知D为HOCH
2CH
2CH
2COOH,F能与溴发生反应得到G,G发生消去反应生成J,J分子中所有碳原子在一条直线上,则J存在-C≡C-三键,结合C的所有碳原子在同一平面上,可知C、E、F中含有C=C双键,综上分析,可推知C为OHC-CH=CH-COONa,顺推可得E为NH
4OOC-CH=CH-COONa,F为HOOC-CH=CH-COOH,G为HOOCCHBrCHBrCOOH,J为HOOC-C≡C-COOH.烃的含氧衍生物A的蒸气密度是相同条件下H
2的88倍,则其相对分子质量=88×2=176,结合C的结构可知H的相对分子质量=176+18-100=94,而H为酚类,可知H为

,B为苯酚钠,故A为
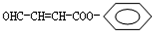
,
(1)A为
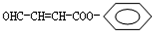
,分子中含有的官能团有:醛基、碳碳双键、酯基;
A→B+C的反应方程式为:
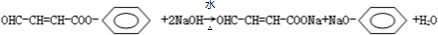
,
故答案为:醛基、碳碳双键、酯基;
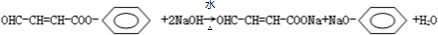
;
(2)由B生成H的反应方程式为:
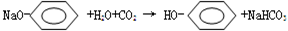
,
故答案为:
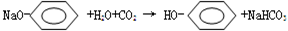
;
(3)由D生成(C
4H
6O
2)
n的反应类型为:缩聚反应,由G到J的反应类型为:消去反应,故答案为:缩聚反应;消去反应;
(4)G的结构简式为:HOOCCHBrCHBrCOOH,故答案为:HOOCCHBrCHBrCOOH;
(5)A为
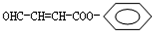
,其同分异构体满足下列条件(不考虑立体异构):①含苯环; ②含羧基;③含醛基; ④含碳碳双键,
含有1个侧链,可以为HOOC-CH=C(CHO)-,HCOOC(CHO)=CH-,OCH-CH=C(COOH)-,有3种,
含有2个侧链,可以为-CHO、-CH=CHCOOH,有邻、间、对3种,可以为-CHO、-C(COOH)=CH
2,有邻、间、对3种,可以为-COOH、-CH=CH-CHO,有邻、间、对3种,可以为-COOH、-C(CHO)=CH
2,有邻、间、对3种,
含有3个侧链,为-CHO、CH
2=CH-、-COOH,若-CHO、CH
2=CH-处于邻位,-COOH有4种位置,若-CHO、CH
2=CH-处于间位,-COOH有4种位置,若-CHO、CH
2=CH-处于对位,-COOH有2种位置,
故符合条件的同分异构体有:3+3×4+4+4+2=25种,
故答案为:25


 ,B为苯酚钠,故A为
,B为苯酚钠,故A为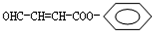 ,据此解答.
,据此解答. ,B为苯酚钠,故A为
,B为苯酚钠,故A为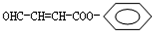 ,
,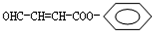 ,分子中含有的官能团有:醛基、碳碳双键、酯基;
,分子中含有的官能团有:醛基、碳碳双键、酯基;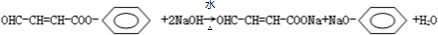 ,
,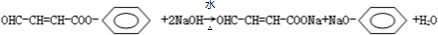 ;
;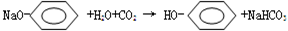 ,
,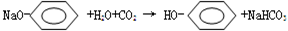 ;
;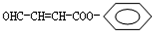 ,其同分异构体满足下列条件(不考虑立体异构):①含苯环; ②含羧基;③含醛基; ④含碳碳双键,
,其同分异构体满足下列条件(不考虑立体异构):①含苯环; ②含羧基;③含醛基; ④含碳碳双键,

 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
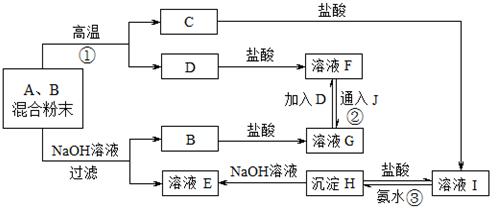
轻巧夺冠周测月考直通高考系列答案 的合成路线流程图(无机试剂任用).合成路线流程图如图:
的合成路线流程图(无机试剂任用).合成路线流程图如图:



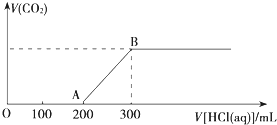 向100mL 3mol?L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.
向100mL 3mol?L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.