
下列叙述正确的是
A.48gO3气体含有6.02×1023个分子
B.常温常压下,2.8 g NO气体含有1.81×1023个原子
C.1L 0.5 mol·L-1 HCl溶液中含有3.01×1023个分子
D.标准状况下,33.6L H2O含有9.03×1023个分子
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年宁夏高二上月考二化学卷(解析版) 题型:选择题
下列试纸使用时,不宜先用水润湿的是( )
A. pH试纸 B. 红色石蕊试纸 C. 淀粉碘化钾试纸 D. 蓝色石蕊试纸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上月考二化学卷(解析版) 题型:选择题
下列离子方程式的书写正确的是
A.氯化亚铁溶液中通入少量氯气:Cl2+Fe2+=Fe3++2Cl-
B.NaHCO3溶液与NaOH溶液反应:OH-+HCO3 -=CO32-+H2O
-=CO32-+H2O
C.钠和冷水反应:Na+2H2O=Na++2OH-+H2↑
D.氯化铝溶液中加入过量的氨水:Al3++4NH3·H2O=AlO2-+4NH4++2H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中化学卷(解析版) 题型:选择题
下列物质的性质描述正确的是
A.Fe在Cl2中燃烧生成FeCl2和FeCl3
B.Na2O2与H2O反应中,Na2O2只作氧化剂
C.FeCl3溶液能与Cu反应,可用蚀刻印刷电路
D.汽车尾气中CO与NO反应生成NO2和CO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中化学卷(解析版) 题型:选择题
下列实验操作中各装置能达到实验目的的是
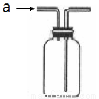

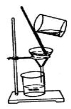
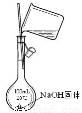
A B C D
A.当装置广口瓶中充满饱和NaCl溶液,从a进气可以收集Cl2气体
B.该装置用于Fe与浓硝酸制取氢气气体的发生装置
C.该装置可以用于分离氢氧化铁胶体中NaCl
D.配制1mol•L-1NaOH溶液100mL
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上期中化学卷(解析版) 题型:填空题
已知在150℃时,NO2按下式发生分解反应2NO2 2NO+O2 △H>0。向容积为1L的密闭容器中加入0.05molNO2在150℃时充分反应,达到平衡后测得c(NO)=0.04mol/L,吸收热量akJ。
2NO+O2 △H>0。向容积为1L的密闭容器中加入0.05molNO2在150℃时充分反应,达到平衡后测得c(NO)=0.04mol/L,吸收热量akJ。
(1)能说明上述反应已经达到化学平衡状态的是 。
A.容器内气体的颜色不再变化
B.容器内压强不再变化
C.容器内气体的密度 不再变化
不再变化
D.容器内气体的平均摩尔质量不再变化
E.v逆(NO2)=v正(NO)
F.相同时间内每消耗2个NO2分子的同时,生成2个NO分子
(2)下列有关该反应的图像中正确的是 。
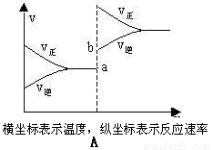
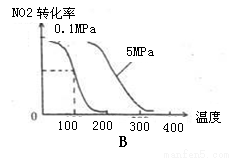
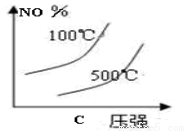

(3)若从反应开始至c(NO)=0.04mol/L共耗时5分钟,则用O2表示的平均反应速率为 。
(4)150℃时上述反应的平衡常数数值为 (可不写单位)。
(5)若在相同的容器内开始时只加入0.05molNO和0.025molO2,在相同的温度下充分反应达到平衡后,恰好放出akJ的热量,则此时O2的转化率为 。
(6)恒容条件下,下列措施中能使n(NO2)/ n(NO)增大的有 。
A.降低温度 B.充入He气
C.再充入1 mol NO (g)和0.5 mol O2(g) D.使用催化剂
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上期中化学卷(解析版) 题型:选择题
一定温度下,将一定量的A、B气体充入密闭容器,发生反应:A(g)+B(g) xC(?)+3D(?)。反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如下图所示。下列有关说法正确的是
xC(?)+3D(?)。反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如下图所示。下列有关说法正确的是
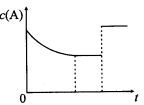
A.x=2,C为气态,D可能为气态也可能为非气态
B.改变的条件可能是使用了催化剂
C.其他条件不变,若向容器中加入少量C,A的平衡转化率不变
D.该反应的化学平衡常数K=[c(C)]2/c(A) ·c(B),且温度升高,K值增大
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
如图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是
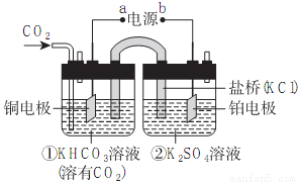
A.该过程是电能转化为化学能的过程
B.铜电极的电极反应式为CO2+8H++8e-=CH4+2H2O
C.一段时间后,①池中n(KHCO3)不变
D.一段时间后,② 池中溶液的pH不一定升高
池中溶液的pH不一定升高
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上月考四化学卷(解析版) 题型:填空题
煤炭是我国的主要能源之一,与之伴生的二氧化硫(SO2)和酸雨污染问题较为突出。目前我国采用的控制方法是电厂烟气脱硫。烟气脱硫的原理是利用碱性物质吸收并固定酸性的二氧化硫,主要有如下两种方法:
I、钠碱循环法脱硫技术。
(1)此法是利用Na2SO3溶液可脱除烟气中的SO2。Na2SO3可由NaOH溶液吸收SO2制得,该反应的离子方程式: 。
(2)NaOH溶液吸收SO的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
①由上表判断,NaHSO3溶液显 性,用化学平衡原理解释: 。
②当溶液呈中性时,离子浓度关系正确的是(选填字母): 。
a.c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3)
b.c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-)
c.c(Na+)=2c(SO32-)+c(HSO3-)
II、石灰石脱硫法
此法是以石灰石为原料通过系列反应将硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g)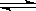 CaO(s)+SO2(g)+CO2(g)△H=218.4kJ·mol-1(反应Ⅰ)
CaO(s)+SO2(g)+CO2(g)△H=218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g)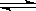 CaS(s)+4CO2(g)△H2=-175.6kJ·mol-1(反应Ⅱ)
CaS(s)+4CO2(g)△H2=-175.6kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)结合反应Ⅰ、Ⅱ写出CaSO4(s)与CaS(s) 的热化学反应方程式 。
(2)对于气体参与的反应,表示平衡常数 Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅰ的Kp= (用表达式表示)。
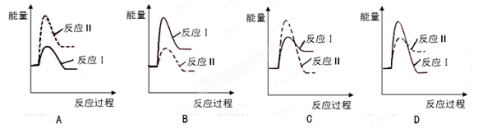
(3)假设某温度下,反应Ⅰ的速率(v1)小于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是 。
(4)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中产生的SO2生成量的措施有 。
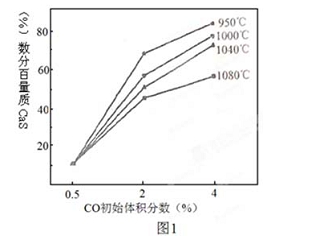
A、向该反应体系中投入生石灰
B、在合适的温度区间内控制较低的反应温度
C、降低CO的初始体积百分数
D、提高反应体系的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com