
如图所示,x、y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色、无味的气体放出。符合这一情况的是下表中的
| a极板 | b极板 | x电极 | z溶液 | |
| A | 锌 | 石墨 | 负极 | CuSO4 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 银 | 铁 | 正极 | AgNO3 |
| D | 铜 | 石墨 | 负极 | CuCl2 |
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工、太阳能电池制造和液晶显示器制造中得到广泛应用。NF3沸点-129 ℃,可在铜的催化作用下由F2和过量NH3反应得到。
(1) NF3分子构型: ,N原子杂化方式: 。
(2)写出制备 NF3的化学反应方程式: 。
(3)NF3的沸点比NH3的沸点(-33 ℃)低得多的主要原因是 。
(4)理论上HF、NaAlO2和NaCl按6∶1∶2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,则该物质的化学式为 。
(5)1~36元素中原子核外电子排布未成对电子数最多的元素其外围电子排布式为_____,有_________个能级;某元素原子的价电子为3d14s2,元素名称为_________,最高正化合价为_______;请写出有2个能层且p轨道中只有一个成对电子的基态原子的外围电子排布图__________________。
(6)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1 ),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①若以上五种元素为前四周期元素,则R为_____________。(填元素符号)
②若五种元素为主族元素,则T为__________区元素。
③若T为第三周期元素,E是第三周期元素中原子半径最小的元素,则T、E形成化合物的空间构型为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知汽车尾气无害化处理反应为2NO(g)+2CO(g)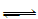 N2(g)+2CO2(g),下列说法中正确的是 ( )
N2(g)+2CO2(g),下列说法中正确的是 ( )
A.使用适当的催化剂不改变反应速率 B.降低压强能提高反应速率
C.升高温度能提高反应速率 D.改变压强对反应速率无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的两个实验装置中,溶液的体积均为200 mL,开始时电解质溶液的浓度均为0.1 mol/L,工作一段时间后,测得导线上均通过0.02 mol电子,若不考虑溶液体积的变化,则下列叙述中正确的是 ( )
A.产生气体的体积:(1) > (2)
 B.电极上析出物质的质量:(1) > (2)
B.电极上析出物质的质量:(1) > (2)
C.溶液pH的变化:(1)增大,(2)减小
D.电极反应式:(1)中阳极:4OH--4e-===2H2O+O2↑,
(2)中负极:2H++2e-===H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
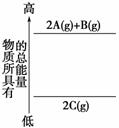
分析右面的能量变化示意图,确定下列选项中正确的是
A.2A(g)+B(g)===2C(g) ΔH<0
B.2A(g)+B(g)===2C(g) ΔH>0
C.2A+B===2C ΔH<0
D.2C===2A+B ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极实现电解,下列说法正确的是
A.电解稀硫酸溶液,实质上是电解水,故溶液pH不变
B.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小
C.电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1∶2
D.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了断裂某些化学键所需的能量:
| 化学键 | H—H | Cl-Cl | I—I | O==O | O—H | H-Cl | H—I |
| 断裂1 mol化学键所吸收的能量(kJ) | 436 | 247 | 151 | x | 463 | 431 | 299 |
请回答下列问题:
(1)如图表示某反应的能量变化关系图,此反应为________(填 “放热”或“吸热”)反应,其中ΔH=________kJ·mol-1(用含C和D的字母表示)。
(2)若此能量变化关系图表示反应H2(g)+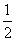 O2(g)===H2O(g)
O2(g)===H2O(g)
ΔH=-241.8 kJ·mol-1,则B=__________kJ·mol-1,x=
________。
(3)表示Cl2与HI气体反应生成碘蒸气与氯化氢的热化学方程式为___________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3 = K2O+5Na2O+16N2↑。若1 mol KNO3反应,则下列说法正确的是
A.N2是还原产物
B.KNO3被氧化
C.转移电子的物质的量为5 mol
D.被氧化的N原子的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对于25℃时pH为12的氨水,叙述正确的是( )
A.由水电离出的c(OH-)=1.0×10-2mol·L-1
B.c(NH )+c(NH3·H2O)=1.0×10-12mol·L-1
)+c(NH3·H2O)=1.0×10-12mol·L-1
C.与等体积、pH=2的盐酸混合后所得的溶液中:
c(NH )>c(OH-)>c(Cl-)>c(H+)
)>c(OH-)>c(Cl-)>c(H+)
D.加入一定量pH=2的醋酸溶液混合后所得的溶液中:c(CH3COO-)+c(OH-)=c(NH )+c(H+)
)+c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com