
| A. | 100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 | |
| B. | 室温下,向pH=3的醋酸溶液加水稀释后,溶液中所有离子浓度均减小 | |
| C. | 向含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 | |
| D. | 向CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
分析 A.100℃时水的离子积常数KW=10-12,则pH=12的NaOH溶液中c(NaOH)=1 mol/L,等体积混合后溶液显碱性;
B.KW只与温度有关,温度不变时水的离子积c(H+)•c(OH-)的值不变,而醋酸稀释时c(H+)减小,则c(OH-)增大;
C.BaSO4在溶液中存在沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq),加入Na2SO4固体后c(SO42-)增大平衡左移,c(Ba2+)减小;
D.CH3COONa溶液存在水解平衡:CH3COO-+H2O?CH3COOH+OH-,则c(Na+)>c(CH3COO-),若加入适量CH3COOH,平衡左移,溶液中c(CH3COO-)增大,则满足c(Na+)=c(CH3COO-),
解答 解:A.100℃时,水的离子积常数KW=10-12,所以pH=12的NaOH溶液c(NaOH)=1 mol/L,pH=2的盐酸c(HCl)=0.01 mol/L,等体积混合后溶液显碱性,故A错误;
B.由于KW只与温度有关,若温度不变时,c(H+)•c(OH-)的值不变,所以醋酸稀释时溶液中c(H+)减小、c(OH-)增大,故B错误;
C.含有BaSO4沉淀的溶液中存在沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO42-(aq),加入Na2SO4固体,c(SO42-)增大,平衡左移,c(Ba2+)减小,故C错误;
D.CH3COONa溶液存在水解平衡:CH3COO-+H2O?CH3COOH+OH-,所以c(Na+)>c(CH3COO-),加入适量CH3COOH,平衡左移,c(CH3COO-)增大,则可使c(Na+)=c(CH3COO-),故D正确;
故选D.
点评 本题考查了弱电解质的电离平衡及其影响、难溶物溶解平衡的应用,题目难度中等,注意掌握影响电离平衡的因素,明确难溶物溶解平衡及其影响,试题培养了学生的灵活应用能力.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:多选题
| A. | 加热 | B. | 加入催化剂 | C. | 减小压强 | D. | 增加C的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
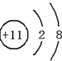 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖水解(用稀H2SO4作催化剂)后的溶液中直接加少量新制Cu(OH)2加热有砖红色沉淀产生 | |
| B. | 将铁屑、溴水、苯混合制溴苯 | |
| C. | 在苯中滴入浓硝酸制硝基苯 | |
| D. | 将铜丝在酒精灯加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. ,A2C的结构式:H-O-H.
,A2C的结构式:H-O-H. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{6}^{12}$C和${\;}_{6}^{13}$C | B. | 金刚石和石墨 | ||
| C. | CH3CH=CH2和环丙烷 | D. | 丁烷和异丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应的平衡常数越大,反应进行的速率越快 | |
| B. | 加热、蒸干NaAlO2溶液和AlCl3溶液,并灼烧都得到Al2O3 | |
| C. | CH3COOH 溶液加水稀释后,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$的值不变 | |
| D. | 0.1mol•L-1CH3COONa溶液中加入少量固体NaOH,碱性增强,平衡向水解方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com