
【题目】下列四图中,曲线变化情况与所给反应(a、b、c、d均大于0)相对应的是
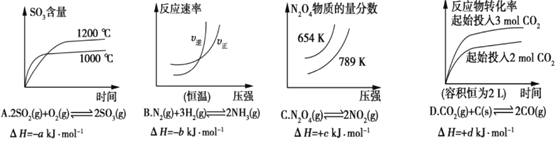
A. A B. B C. C D. D.
【答案】C
【解析】A项,1200℃时反应速率大于1000℃时反应速率,1200℃先达到平衡,但图中1000℃先达到平衡,不符合平衡的建立,错误;B项,对反应N2(g)+3H2(g)![]() 2NH3(g),增大压强,正反应速率、逆反应都加快,达到平衡后增大压强平衡向正反应方向移动,υ正
2NH3(g),增大压强,正反应速率、逆反应都加快,达到平衡后增大压强平衡向正反应方向移动,υ正![]() υ逆,与曲线不一致,错误;C项,对反应N2O4(g)
υ逆,与曲线不一致,错误;C项,对反应N2O4(g)![]() 2NO2(g),温度一定时,增大压强平衡向逆反应方向移动,N2O4物质的量分数增大,压强一定时,升高温度平衡向正反应方向移动,N2O4物质的量分数减小,与曲线一致,正确;D项,由于C为固态,对反应CO2(g)+C(s)
2NO2(g),温度一定时,增大压强平衡向逆反应方向移动,N2O4物质的量分数增大,压强一定时,升高温度平衡向正反应方向移动,N2O4物质的量分数减小,与曲线一致,正确;D项,由于C为固态,对反应CO2(g)+C(s)![]() 2CO(g),恒容容器中增加CO2物质的量相当于增大压强平衡向逆反应方向移动,反应物的转化率减小,与曲线不一致,错误;答案选C。
2CO(g),恒容容器中增加CO2物质的量相当于增大压强平衡向逆反应方向移动,反应物的转化率减小,与曲线不一致,错误;答案选C。


科目:高中化学 来源: 题型:
【题目】金属铝分别和O2、O3发生反应生成Al2O3 , 反应过程和能量关系如下图所示(图中的ΔH表示生成1 mol产物的数据)。下列有关说法中不正确的是( )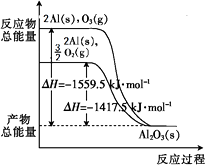
A.Al(s)与O3(g)反应的热化学方程式为2Al(s)+O3(g)=Al2O3(s) ΔH =-1559.5 kJ·mol-1
B.等质量的O2比O3的能量低
C.1 mol O2完全转化为O3 , 需吸收142 kJ的热量
D.给3O2(g) ![]() 2O3(g)的平衡体系加热,有利于O3的生成
2O3(g)的平衡体系加热,有利于O3的生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一固定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2 ![]() 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量的NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2 , 气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。请回答下列问题(计算结果保留一位小数):
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量的NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2 , 气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。请回答下列问题(计算结果保留一位小数):
(1)判断该反应达到平衡状态的标志是。(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.向装置中再充入SO3
(3)求该反应达到平衡时SO2的转化率为(用百分数表示)。
(4)若将平衡混合气体的5%通入过量的Ba(OH)2溶液,生成沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中有错误的是( )
A. 某原子K层上只有一个电子 B. 某离子M层和L层上的电子数均为K层的4倍
C. 某原子M层上的电子数为L层电子数的4倍 D. 存在核电荷数与最外层电子数相等的离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL H2SO4与CuSO4的混合液中,用石墨作电极电解,两极上均收集到2.24L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
A.0.5 mol/L
B.1 mol/L
C.3 mol/L
D.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10 mL 0.1mol/LNaOH溶液中加入0.1mol/L的一元酸HA溶液pH的变化曲线如图所示。下列说法正确的是( )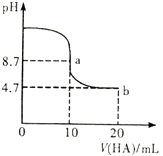
A.a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,c(Na+)=c(A-)+c(HA)
D.b点所示溶液中c(A-)>c(HA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,按化合物、单质、混合物顺序排列的是( )
A.烧碱、液态氧、碘酒B.生石灰、白磷、熟石灰
C.干冰、水银、氯化氢D.空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氧化还原反应的叙述正确的是
A.氧化还原反应的本质是元素化合价发生变化
B.物质所含元素化合价降低的反应是氧化反应
C.置换反应一定属于氧化还原反应
D.化合反应和分解反应不可能是氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com