
(1)通过点燃的方法可以鉴别聚乙烯和聚氯乙烯。如果塑料点燃时有强烈的刺激性气味,这种塑料可能是由 制成的。
(2)某同学设计了如图所示实验来验证塑料燃烧的产物。
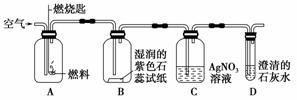
若A瓶燃烧的是聚氯乙烯塑料,在B瓶中可以看到的现象是________________________________________________________________________,
C、D两瓶中发生反应的化学方 程式为____
程式为____ ____________________________________________________________________。
____________________________________________________________________。
若A瓶中 用的是聚乙烯塑料,则在C瓶中 (“能”或“不能”)观察到沉淀。
用的是聚乙烯塑料,则在C瓶中 (“能”或“不能”)观察到沉淀。
科目:高中化学 来源: 题型:
下列说法正确的是 ( )。
A.卧室的地面有时要铺地毯,地毯具有隔音隔热、柔软舒适、色彩艳丽等特点
B.复合木地板比实木地板环保
C.黏合剂都属于高分子合成材料
D.合成胶水是天然黏合剂
查看答案和解析>>
科目:高中化学 来源: 题型:
用Pt作电极,电解100 mL 0.4 mol·L-1的NaCl溶液和100 mL 0.1 mol·L-1的稀硫酸,标准状况下产生0.224 L Cl2时停止电解,取出电极,将两烧杯溶液混合并冷却至常温,所得溶液的pH为(设气体产物全部逸出,混合溶液的总体积为200 mL)( )
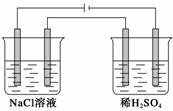
A.5 B.6 C.7 D.13
查看答案和解析>>
科目:高中化学 来源: 题型:
如图,烧杯中试管内有一枚铁钉,放置数天观察:
(1)铁钉在逐渐生锈,则铁钉的腐蚀属于 腐蚀。(2)若试管内液面上升 ,则原溶液呈 ,发生 腐蚀,电极反应:负极 ;正极 。
,则原溶液呈 ,发生 腐蚀,电极反应:负极 ;正极 。
(3)若试管内液面下降,则原溶液呈 性,电极反应:负极 ;正极 。
查看答案和解析>>
科目:高中化学 来源: 题型:
橡胶属于重要的工业原料。它是一种有机高分子化合物,具有良好的弹性,但强度较差。为了增强某些橡胶制品的强度,加工时往往需硫化处理,即将橡胶原料与硫黄在一定条件下反应。橡胶制品硫化程度越高,强度越大,弹性越差。下列橡胶制品中,加工时硫化程度较高的是 ( ) 。
。
A.橡皮筋 B.汽车外胎
C.普通气球 D.医用乳胶手套
查看答案和解析>>
科目:高中化学 来源: 题型:
硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(DGa与B同主族,Ga的基态原子核外电子排布式为
第一电离能由大到小的顺序是
(2)硼酸(H3B03)是白色片状晶体(层状结构如右图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
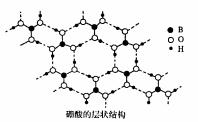
①硼酸中B原子的杂化轨道类型为 。
②硼酸晶体中存在的作用力有范德华力和 。
③加热时,硼酸的溶解度增大,主要原因是 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OHˉ 而呈酸性。写出硼酸的电离方程式_ 。
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理 。 [BH4]-的空问构型是____。
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式 。
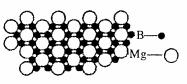
(5)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,右图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为 。
(6)金刚石的晶胞如右图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5pm,则立方氮化硼的密度是____g· cmˉ 3
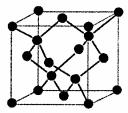
(只要求列算式,不必计算出数值,阿伏伽德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )。
A.乙醇和汽油都是可再生能源,应大力推 广“乙醇汽油”
广“乙醇汽油”
B.钢铁在 海水中比在河水中更易腐蚀,主要原因是海水中含氧量高于河水
海水中比在河水中更易腐蚀,主要原因是海水中含氧量高于河水
C.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源
D.凡含有食品添加剂的食物对人体健康均有害,不宜食用
查看答案和解析>>
科目:高中化学 来源: 题型:
明矾石的主要成分是K2SO4·Al2(SO4)3·2Al 2O3·6H2O,此外还含有少量Fe2O3杂质。利用明矾石来制取纯净的Al2O3、K2FeO4和H2SO4的工艺流程如图所示:
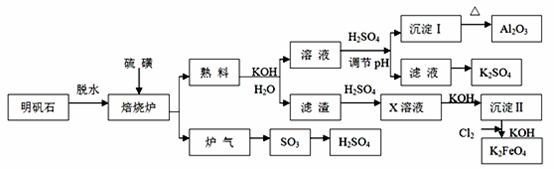
(1)“焙烧”过程中Al2(SO4)3和S发生反应的化学方程式为 ;
若生成102g Al2O3,转移的电子数目为 ;
(2)生成沉淀Ⅰ时的离子方程式为 ;
(3)写出化学式:沉淀Ⅱ是 ;
(4)溶液经加硫酸调节pH后,过滤,洗涤,可得沉淀Ⅰ,证明沉淀Ⅰ已洗涤干净的实验操作和现象是 ;
(5)从滤液中得到K2SO4晶体的方法是 ;
(6)K2FeO4也可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取K2FeO4的阳极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com