
| A. | 化学反应不一定有分子碰撞 | B. | 化学反应的活化能一定大于零 | ||
| C. | 具有较高能量的分子是活化分子 | D. | 发生有效碰撞的分子是活化分子 |
分析 活化分子的能量比普通分子高,不同的化学反应需要的活化能差别很大,有些分子可能能量很高了,但不一定是该反应的活化分子,物质发生化学反应,必须分子间发生有效碰撞,有效碰撞的条件:①活化分子,②有合适的取向,据此分析.
解答 解:A.能发生化学反应的碰撞是有效碰撞,所以化学反应一定有分子碰撞,故A错误;
B.活化能等于0的化学反应应该是不存在的,但是有接近0的如铯与水反应活化能一定是正的,但是活化能是0,这说明这个反应处在平衡点,故B错误;
C.不同反应活化分子的能量差距很大,具有较高能量的分子未必是活化分子,故C错误;
D.发生有效碰撞的分子一定是能量比较高的活化分子,能量比较低的普通分子,不能发生有效碰撞,故D正确;
故选D.
点评 本题主要考查了有效碰撞、化学反应的本质等,难度中等,根据课本知识即可完成.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源: 题型:多选题
| A. | pH=5的NH4Cl溶液或醋酸中,由水电离出的c(H+)均为10-9 mol/L | |
| B. | pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7 | |
| C. | pH=3的醋酸溶液加水稀释过程中:$\frac{c(O{H}^{-})}{c({H}^{+})}$逐渐增大 | |
| D. | 0.1 mol/L Na2CO3溶液和0.1 mol/L NaHSO4溶液等体积混合,溶液中c(Na+)+c(H+)=2c(CO32-)+2c(SO42-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
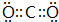 ,B与D形成的原子个数比为1:1的化合物的电子式是
,B与D形成的原子个数比为1:1的化合物的电子式是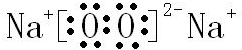 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 -R、-R′为可能相同或可能不同的原子或原子团
-R、-R′为可能相同或可能不同的原子或原子团 ,X中核磁共振氢谱峰面积比是2:1.
,X中核磁共振氢谱峰面积比是2:1. ,反应类型是加聚反应.
,反应类型是加聚反应. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀HNO3 | B. | CuSO4溶液 | C. | FeCl3溶液 | D. | AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.请回答下列问题:
如图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com