
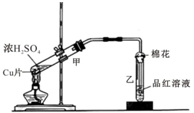
 如图为浓硫酸与铜片反应的装置.请回答:
如图为浓硫酸与铜片反应的装置.请回答:分析 (1)铜与浓硫酸反应生成硫酸铜、二氧化硫和水,据此写出反应的化学方程式;
(2)二氧化硫能使品红溶液褪色,但二氧化硫的漂白性不稳定,加热时会恢复原来的颜色;
(3)A.该反应中浓硫酸只体现酸性和氧化性;
B.试管乙中含有碱液的棉花,防止二氧化硫散失到空气中,造成大气污染;
C.反应一段时间后,将试管甲中的溶液缓慢倒入盛有水的烧杯,含有铜离子的溶液,溶液显蓝色;
D.含0.04mol溶质的浓硫酸与足量的铜片反应,随着反应的进行浓度减小,稀硫酸与铜不反应.
解答 解:(1)铜与浓硫酸反应的化学方程式为:Cu+2H2SO4$\frac{\underline{\;加热\;}}{\;}$CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4$\frac{\underline{\;加热\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)二氧化硫能和有色物质生成无色物质,二氧化硫能使品红溶液褪色,所以二氧化硫具有漂白性;但生成的无色物质不稳定,加热时会恢复原来的颜色;
故答案为:品红溶液褪色;
(3)A.该反应中浓硫酸只体现酸性和氧化性,故A错误;
B.试管乙中含有碱液的棉花,防止二氧化硫散失到空气中,造成大气污染,其作用是吸收过量的SO2,防止环境污染,故B正确;
C.反应一段时间后,将试管甲中的溶液缓慢倒入盛有水的烧杯,含有铜离子的溶液,溶液显蓝色,故C正确;
D.含0.04mol溶质的浓硫酸与足量的铜片反应,随着反应的进行浓度减小,稀硫酸与铜不反应,所以收集到SO2的体积在标准状况小于448mL,故D错误;
故选:AD.
点评 本题考查了浓硫酸的化学性质、二氧化硫的性质及检验方法,题目难度中等,注意掌握浓硫酸的化学性质,明确二氧化硫的漂白性是暂时的,加热时会恢复原来的颜色.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
某非金属单质A和氧气发生化合反应生成B。为气体,其体积是反应掉氧气体积的两倍(同温、同压)。以下对B的分子组成的推测一定正确的是( )
A.有1个氧原子 B.有2个氧原子 C.有1个A原子 D.有2个A原子
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电镀铜时用待镀的金属制品作阳极、铜作阴极 | |
| B. | AlCl3熔点低,电解熔融AlCl3冶炼铝更节能 | |
| C. | 电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 | |
| D. | 氯碱工业实际是指电解饱和食盐水的工业生产 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
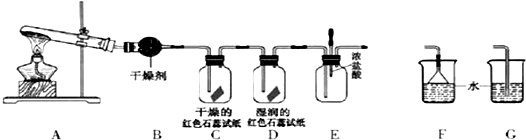
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上10月月考化学试卷(解析版) 题型:选择题
配制物质的量浓度为0.1 mol/L的Na2CO3溶液l00mL时,下列操作正确的是( )
A. 用托盘天平称取l.06g无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 定容时,若仰视,则所配溶液的浓度将偏高
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物可能含共价键 | B. | 共价化合物不可能含离子键 | ||
| C. | 离子化合物中一定含离子键 | D. | 共价化合物中不含离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com