
| A. | Ca2+ | B. | K | C. | S2- | D. | K+ |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4电离方程式H2SO4=2H++S6++4O2- | |
| B. | H2、D2、T2互为同位素 | |
| C. | 18g H2O含有的电子数为10NA | |
| D. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm的核外电子数和中子数均为62 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3H4和C3H6O | B. | C3H6和C3H8O2 | C. | C3H6O2和C3H8O | D. | C3H8O和C4H6O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:1 | B. | 5:1 | C. | 1:3 | D. | 1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 煤的干馏和石油的分馏均属化学变化 | |
| C. | BaSO4在医学上用作钡餐,Ba2+对人体无毒 | |
| D. | 14C可用于文物的年代鉴定,12C与14C互为同素异形体. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 42% | B. | 60% | C. | 70% | D. | 80% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 物质 | △H(kJ/mol) |
| CO(g) | -283.0 |
| CH4(g) | -890.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 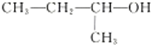 的名称为2-甲基-1-丙醇 的名称为2-甲基-1-丙醇 | |||||||||||||||||
| B. | 按照以下的排布规律,第15项物质可能与金属钠反应
| |||||||||||||||||
| C. | 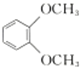 在核磁共振氢谱中出现两组峰,其氢原子个数之比为3:2 在核磁共振氢谱中出现两组峰,其氢原子个数之比为3:2 | |||||||||||||||||
| D. | 甲苯分子内所有原子均在同一平面 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com