
| A. | 天然弱碱性水呈碱性的原因是其中含有较多的Mg2+、Ca2+等离子 | |
| B. | 食用地沟油对人体的危害极大,原因主要是里面含有黄曲霉素和甘油三酯 | |
| C. | 地球上CH4、CO2等气体含量上升容易导致温室效应,进而引发灾难性气候 | |
| D. | 保鲜膜、一次性食品袋的主要成分是聚氯乙烯 |
分析 A.天然水呈弱碱性的原因是水中存在弱酸的阴离子,阴离子水解结合水电离出的氢离子;
B.地沟油中含有黄曲霉素、苯并芘,这两种毒素都是致癌物质,甘油三酯是高级脂肪酸酯;
C.CH4、CO2等均可导致全球温度升高;
D.食品保鲜膜、一次性食品袋的主要成分是聚乙烯.
解答 解:A.天然水呈弱碱性,是因为天然水中有CO32-或HCO3-它们水解使水呈弱碱性,其离子方程式为CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-,不能含较多的Mg2+、Ca2+等离子,故A错误;
B.地沟油中含有黄曲霉素、苯并芘两种毒素,它们都是致癌物质,故食用地沟油对人体的危害很大,故B错误;
C.CH4、CO2等均可导致全球温度升高,导致温室效应,进而引发灾难性气候,故C正确;
D.食品保鲜膜、一次性食品袋的主要成分是聚乙烯,不能使用聚氯乙烯,聚氯乙烯使用时释放有毒物质对人体有害,故D错误;
故选C.
点评 本题考查物质的性质与用途,为高频考点,把握物质的性质、化学与生活及环境的关系、性质与用途的关系等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3CH3+Cl2$\stackrel{光照}{→}$CH3CH2Cl+HCl | |
| B. | CH2=CH2+HBr→CH3CH2Br | |
| C. |  | |
| D. | CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 探究Na与水反应可能有O2生成 | |
| B. | 探究Na2O2与SO2反应可能有Na2SO4生成 | |
| C. | 探究浓硫酸与铜在一定条件下反应产生的黑色物质中可能含有CuS | |
| D. | 探究向滴有酚酞的NaOH溶液中通入Cl2,溶液红色褪去的原因是溶液酸碱性改变所致,还是HClO的漂白性所致 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO | B. | N2O3 | C. | NO2 | D. | N2O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该铅蓄电池正在充电 | |
| B. | 工作一段时间后,溶液的pH不断减小 | |
| C. | a为铅蓄电池的正极 | |
| D. | b电极发生的反应为PbO2+4H++SO42-+2e-═PbSO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
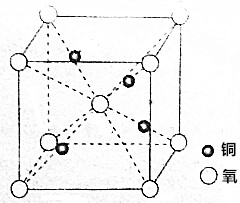 铜的一种氧化物在陶瓷涂色等方面有重要应用,它的晶胞如图所示.
铜的一种氧化物在陶瓷涂色等方面有重要应用,它的晶胞如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 赤铁矿、磁铁矿、黄铁矿、孔雀石都是常见的铁矿石 | |
| B. | 纤维素、PLA(聚乳酸)、维生素C、硝化纤维等都是高分子化合物 | |
| C. | 高容量的储氢材料的研制是推广应用燃料电池的关键问题之一 | |
| D. | 将呼吸产生的二氧化碳用石灰水吸收符合”低碳经济“原则 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
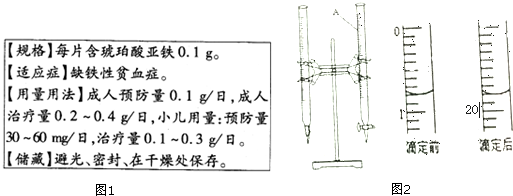
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 现代元素周期表是按照元素相对原子质量由小到大排列而成的 | |
| B. | 同主族的元素,都是按从上到下的顺序电子层数逐渐增多 | |
| C. | 同周期的元素,都是按从左到右的顺序原子最外层电子数由1递增到8 | |
| D. | 同周期的元素的原子和离子半径,都是按从左到右的顺序逐渐减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com