
【题目】实验室制备苯甲醇和苯甲酸的化学原理是: ,
,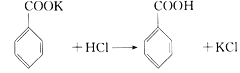 。已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3℃;苯甲酸的熔点为121.7℃,沸点为249℃,常温下,在水中的溶解度为0.34g;乙醚的沸点为34.8℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:
。已知苯甲醛易被空气氧化,苯甲醇的沸点为205.3℃;苯甲酸的熔点为121.7℃,沸点为249℃,常温下,在水中的溶解度为0.34g;乙醚的沸点为34.8℃,难溶于水。制备苯甲醇和苯甲酸的主要过程如下所示:

试根据上述信息回答下列问题:
(1)操作I的名称是________,乙醚溶液中所溶解的主要成分是____________;
(2)操作Ⅱ的名称是________,产品甲是________。
(3)操作Ⅲ的名称是________,产品乙是________。
(4)如图所示,操作Ⅱ中温度计水银球上沿放置的位置应是____(填“a”、“b”、“c” 或“d”),收集乙醚产品的适宜温度为___。

【答案】萃取分液 苯甲醇 蒸馏 苯甲醇 过滤 苯甲酸 b 34.8℃
【解析】
由流程结合题中信息可知,苯甲醛与KOH反应生成白色糊状物为苯甲醇、苯甲酸钾的混合物,然后加水、乙醚萃取苯甲醇,则乙醚溶液中含苯甲醇,操作II为蒸馏,得到产品甲为苯甲醇;水溶液中含苯甲酸钾,加盐酸发生强酸制取弱酸的反应,生成苯甲酸,苯甲酸的溶解度小,则操作Ⅲ为过滤,则产品乙为苯甲酸,据此分析解答。
由流程可知,苯甲醛与KOH反应生成苯甲醇、苯甲酸钾,然后加水、乙醚萃取苯甲醇,则乙醚溶液中含苯甲醇,操作II为蒸馏,得到产品甲为苯甲醇;水溶液中含苯甲酸钾,加盐酸发生强酸制取弱酸的反应,生成苯甲酸,苯甲酸的溶解度小,则操作Ⅲ为过滤,则产品乙为苯甲酸。
(1)据上述分析,操作Ⅰ为萃取、分液;乙醚溶液中的主要成分是苯甲醇,
故答案为:萃取(分液);苯甲醇;
(2)乙醚溶液中含苯甲醇,操作II为蒸馏,得到产品甲为苯甲醇,故答案为:蒸馏;苯甲醇;
(3)水溶液中含苯甲酸钾,加盐酸发生强酸制取弱酸的反应,生成苯甲酸,常温下,在水中的溶解度为0.34g,苯甲酸的溶解度小,则操作Ⅲ为过滤,则产品乙为苯甲酸,故答案为:过滤;苯甲酸;
(4)蒸馏时,温度计的水银球应在蒸馏烧瓶的支管口附近,则温度计水银球的放置位置为b;根据乙醚的沸点为34.8℃可知,需要控制蒸气的温度为34.8℃,故答案为:b;34.8℃。


科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的、以离子形式存在的碘元素。下图是实验室从海藻里提取碘的流程中的一部分。

下列判断正确的是
A. 步骤①③的操作分别是过滤、萃取
B. 可用淀粉溶液检验步骤②的反应是否进行完全
C. 步骤③中加入的有机溶剂是裂化汽油或乙醇
D. 步骤④的操作是过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置进行化学反应X+2Y=2Z能量变化情况的研究。当向试管中滴加试剂Y时,观察到U形管中液面甲处下降、乙处上升。下列关于该反应的叙述正确的是( )
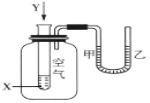
①该反应为放热反应
②该反应为吸热反应
③生成物的总能量比反应物的总能量高
④反应物的总能量比生成物的总能量高
⑤该反应过程可以看成贮存于X、Y内部的部分能量转化为热能而释放出来
A.仅①④⑤B.仅①④C.仅①③D.仅②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有显著抗癌活性的10-羟基喜树碱的结构如图所示,

下列关于10-羟基喜树碱的说法正确的是
A. 10-羟基喜树碱属于芳香烃
B. 分子式为:C20H16N2O5
C. 不能发生酯化反应
D. 一定条件下,1mol该物质可与9molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“软电池”采用一张薄层纸片作为传导体,一面镀Zn,另一面镀MnO2。电池总反应为Zn+2MnO2+H2O=2MnO(OH)+ZnO。下列说法正确的是( )
A.该电池的正极为ZnO
B.Zn电极附近溶液的pH不变
C.电池正极的电极反应为2MnO2+2e-+2H2O=2MnO(OH)+2OH-
D.当0.1molZn完全溶解时,流经电解液的电子的物质的量为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】简单原子的原子结构可用下图形象的表示:其中●表示质子或电子,O表示中子,则下列有关的叙述正确的是
![]()
A.①②③是三种化学性质不同的粒子。
B.①②③具有相同的质量数.
C.①②③为同素异形体
D.①②③互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应A(g)+ 3B(g)![]() 2C(g), 下列说法能证明这一 反应已经达到化学平衡状态的是
2C(g), 下列说法能证明这一 反应已经达到化学平衡状态的是
A.生成C的速率与分解C的速率相等.
B.A. B、C的分子数之比为1:3:2
C.A、B、C的浓度相等
D.单位时间消耗nmolA,同时生成2nmolC
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(7分)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A![]() H++HA- HA-
H++HA- HA-![]() H++A2-
H++A2-
试完成下列问题:
(1)Na2A溶液显 (填“酸性”“中性”或“碱性”)。理由是
(用离子方程式表示)。
(2)在0.1 mol·L-1的Na2A溶液中,下列粒子浓度关系式正确的是 。A.c(A2-)+c(HA-)+c(H2A)=0.1 mol·L-1
B.c(OH-)=c(H+)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
(3)已知0.1 mol·L-1 NaHA溶液的pH=2,则0.1 mol·L-1H2A溶液中氢离子的物质的量浓度可能是 0.11 mol·L-1(填“<”、“>”或“=”),理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮化合物与生产、生活、生命和环境息息相关。
(1)NO加速臭氧层被破坏,其反应过程如图所示。
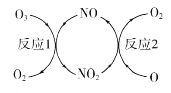
①NO的作用是________________________。
②已知:O3(g)+O(g) =2O2(g) △H=-143kJ·mol-1
反应l:O3(g)+NO(g) =NO2(g)+O2(g)△H1=-200.2kJ·mol-1
则反应2的热化学方程式为____________________________。
(2)肌红蛋白(Mb)是肌肉内储存氧的蛋白质,构成肌红蛋白的甘氨酸(H2NCH2COOH)是一种两性物质,在溶液中以三种离子形式存在,其转化关系如下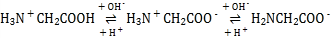 三种离子的物质的量分数(δ)与[
三种离子的物质的量分数(δ)与[![]() ]的关系如图所示。
]的关系如图所示。
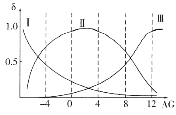
①溶液呈中性时,三种离子浓度由大到小的顺序为______________________。
②向AG=12的溶液中加入过量NaOH溶液时,主要反应的离子方程式为______________。
(3)肌红蛋白(Mb)可与O2结合生成MbO2:![]() 。37℃时测得肌红蛋白的结合度(α)与p(O2)的关系如下表。
。37℃时测得肌红蛋白的结合度(α)与p(O2)的关系如下表。
[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的物质的量分数]
p(O2)/kPa | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
α(MbO2)% | 50.0 | 66.7 | 80.0 | 85.7 | 88.9 | 90.9 | 92.3 |
①计算37℃时,上述反应的平衡常数K=__________kPa-1(气体和溶液中的溶质分别用分压和物质的量浓度表示)。
②37℃时,若空气中氧气分压为21.0 kPa,则人正常呼吸时α的最大值为________%(保留1位小数)。
③温度不变时,游客在山顶时体内MbO2的浓度比在山下________(填“高”或“低”)。
④研究发现,v正=k正·c(Mb)·p(O2),v逆=k
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com