
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
 已知X、Y、Z、W是短周期中四种非金属元素,它们的原子序数依次增大,X元素原子价电子排布式为ns1,Y元素是空气中含量最多的元素,Z 与W同主族,而且W原子的电子排布式中,p轨道上只有1个未成对电子.
已知X、Y、Z、W是短周期中四种非金属元素,它们的原子序数依次增大,X元素原子价电子排布式为ns1,Y元素是空气中含量最多的元素,Z 与W同主族,而且W原子的电子排布式中,p轨道上只有1个未成对电子.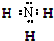
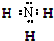
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)通常所说的化石燃料有
(1)通常所说的化石燃料有查看答案和解析>>
科目:高中化学 来源: 题型:
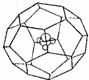
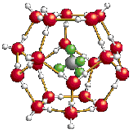 我国在青藏高原发现大储量可燃冰.可燃冰的晶体结构模型如图:
我国在青藏高原发现大储量可燃冰.可燃冰的晶体结构模型如图:查看答案和解析>>
科目:高中化学 来源: 题型:
A.CH4·6H2O B.CH4·8H2O
C.CH4·10H2O D.CH4·14H2O
(2)“冰甲烷”中水分子与甲烷分子以___________相结合形成___________晶体。
(3)由于无水醋酸钠与碱石灰共热可以制得甲烷,你预测将无水苯乙酸钠与碱石灰共热时,所得的有机物主要是___________(填选项的字母)。
A.甲烷 B.甲苯 C.苯甲酸钠、甲烷 D.乙苯
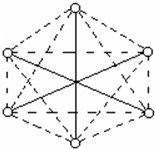
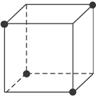
(4)将甲烷分子的4个氢原子互相连接可以构成一个正四面体。如图所示是一个正立方体,设想将一个甲烷分子放入,碳原子将居于正立方体的中心,黑球表示已有1个氢原子居于该立方体的一角,请在图上画上另外三个黑球标出其他3个氢原子的位置。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com