
 ij��ѧ����С����ͼװ��ʹ����Һ�巴Ӧ�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A��A�¶˻����رգ��У�
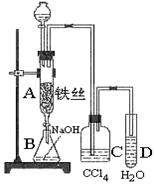
ij��ѧ����С����ͼװ��ʹ����Һ�巴Ӧ�������Һ©���м��뱽��Һ�壬�ٽ����Һ�������뷴Ӧ��A��A�¶˻����رգ��У����� �����巴Ӧ�����廯�������廯���������£������巢��ȡ����Ӧ�����屽��HBr��Cװ�����ڳ�ȥ�壬D����HBr��Ϊ����HBr���ɼ�����������Һ����Ӧ������������������巴Ӧ���ɳ�ȥ�屽�е��壮
���嵥�������������Ʒ�Ӧ���屽���ܣ�
�ڱ���Һ�����廯���������·���ȡ����Ӧ�����屽���廯�䣻
���������Һ�巢������ȡ����Ӧ������HBr���ɣ�����������Ǽӳɷ�Ӧ������HBr���ɣ�
��� �⣺�����巴Ӧ�����廯�������廯���������£������巢��ȡ����Ӧ�����屽��HBr��Cװ�����ڳ�ȥ�壬D����HBr��Ϊ����HBr���ɼ�����������Һ����Ӧ������������������巴Ӧ���ɳ�ȥ�屽�е��壮
���嵥����������������Һ��Ӧ���屽���ܣ����������������Һ���Գ�ȥ�屽�е��嵥�ʣ��ʴ�Ϊ����ȥ�����屽�е��壻
��FeBr3Ϊ��Ӧ�Ĵ����������巴Ӧ�����廯�����ڴ����������£������ϵ���ԭ�ӱ���ԭ����ȡ���������屽��ͬʱ���廯�����ɣ�����ʽΪC6H6+Br2$\stackrel{FeBr_{3}}{��}$C6H5Br+HBr���ʴ�Ϊ��C6H6+Br2$\stackrel{FeBr_{3}}{��}$C6H5Br+HBr��ȡ����Ӧ��
�ۿ���ʯ����Һ�����������ȡ����Ӧ�������ӷ����廯�������е����������廯��ļ����и������ã���ˣ��ڼ����廯��ǰ�����ȥ����������Ҳ����C��ʢ�ŵ�CCl4�����ã�
�ʴ�Ϊ��ʯ����Һ����Һ���ɫ��
���� ���⿼�鱽��ȡ����Ӧ����ʽ��ʵ�������Լ�����HBr�ļ��飬Ϊ��Ƶ���㣬������ѧ���ķ�����ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ�ע�����ձ���ȡ����Ӧԭ������ȷ��Ӧ�IJ��PHBr�Ļ�ѧ���ʽ��н��⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

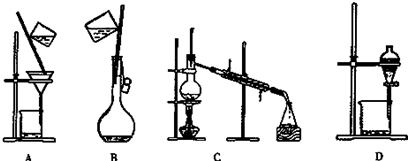
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��X��W��Z | |
| B�� | ����������Ӧˮ��������ԣ�W��R | |
| C�� | ����̬�⻯������ȶ��ԣ�Y��W | |
| D�� | Y�����ڱ��е�λ��Ϊ�ڶ����ڢ�A�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
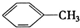 ��
��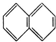 ��
��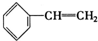 ��C2H4��CH2=CH-CH=CH2��C3H6��
��C2H4��CH2=CH-CH=CH2��C3H6��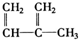 ��
��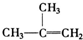
| A�� | �ٺ� �� | B�� | �ܺ͢� | C�� | �ݺ͢� | D�� | �͢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
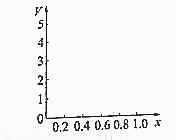
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
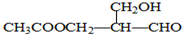 ���л���ķ����У���ij��̼ԭ���������ĸ���ͬ��ԭ�ӻ�ԭ���ţ�����̼ԭ�ӳ�Ϊ������̼ԭ�ӡ�������һ������̼ԭ�ӵ�����һ�����й�ѧ���ԣ���ͼ�����й�ѧ���ԣ��������з�Ӧ�����ɵ��л������й�ѧ���Ե��ǣ�������
���л���ķ����У���ij��̼ԭ���������ĸ���ͬ��ԭ�ӻ�ԭ���ţ�����̼ԭ�ӳ�Ϊ������̼ԭ�ӡ�������һ������̼ԭ�ӵ�����һ�����й�ѧ���ԣ���ͼ�����й�ѧ���ԣ��������з�Ӧ�����ɵ��л������й�ѧ���Ե��ǣ�������| A�� | �� | B�� | �٢ڢܢ� | C�� | �ۢ� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��֪2H2��g��+O2��g��=2H2O��g������H=-483.6 kJ•mol-1������ȼ����Ϊ��H=-241.8 kJ•mol-1 | |
| B�� | ��֪C��ʯī��s��=C�����ʯ��s������H��0����ʯī�Ƚ��ʯ�ȶ� | |
| C�� | ��֪NaOH��ag��+HCl��aq��=NaCl��aq��+H2O��l������H=-57.4 kJ•mol-1��20.0g NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ������ | |
| D�� | ��֪2C��s��+2O2��g���T2CO2��g������H1 2C��s��+O2��g���T2CO��g������H2�����H1����H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com