
【题目】化合物N具有镇痛、消炎等药理作用,其合成路线如下:
![]()
![]()
 →
→
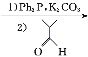
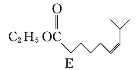
![]()
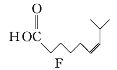
![]()
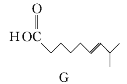
![]()

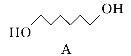
(1)A的系统命名为___________,E中官能团的名称为__________________。
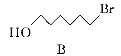
(2)A→B的反应类型为________,从反应所得液态有机混合物中提纯B的常用方法为___________________________。
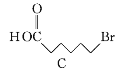
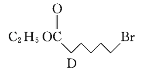
(3)C→D的化学方程式为____________________________________________。
(4)参照上述合成路线,以![]() 为原料,采用如下方法制备医药中间体
为原料,采用如下方法制备医药中间体![]() 。
。
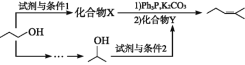
该路线中试剂与条件1为_______________,X的结构简式为___________________;试剂与条件2为______________________,Y的结构简式为_______________。
【答案】1,6-己二醇 碳碳双键、酯基 取代反应 减压蒸馏(或蒸馏)  +C2H5OH
+C2H5OH![]()
 +H2O 试剂与条件1:HBr,加热 X:
+H2O 试剂与条件1:HBr,加热 X:![]() 试剂与条件2:O2/Cu或Ag,加热 Y:
试剂与条件2:O2/Cu或Ag,加热 Y:![]()
【解析】
(1)根据题中已给的A结构简式分析命名,根据E的结构简式判断官能团;
(2)Br原子取代A分子中的1个羟基;液体有机物互溶,不分层,但沸点不同;
(3)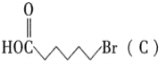 与C2H5OH发生酯化反应生成
与C2H5OH发生酯化反应生成 ,结合酯化反应原理及原子守恒书写方程式;
,结合酯化反应原理及原子守恒书写方程式;
(4) 与HBr发生取代反应;
与HBr发生取代反应;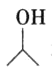 发生催化氧化生成Y(
发生催化氧化生成Y(![]() )。
)。
(1)A为![]() ,其化学名称为1,6己二醇;E为
,其化学名称为1,6己二醇;E为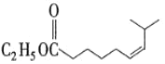 ,所含官能团为酯基和碳碳双键;
,所含官能团为酯基和碳碳双键;
(2)A与HBr反应,Br原子取代A分子中的1个羟基,则A→B是取代反应;液体有机物互溶,不分层,可利用其沸点不同,采用减压蒸馏(或蒸馏)的方法提纯B;
(3) 与C2H5OH发生酯化反应生成
与C2H5OH发生酯化反应生成 ,结合酯化反应原理及原子守恒即可写出化学方程式
,结合酯化反应原理及原子守恒即可写出化学方程式 +C2H5OH
+C2H5OH![]()
 +H2O;
+H2O;
(4) 与HBr在加热的条件下发生取代反应生成化合物X(
与HBr在加热的条件下发生取代反应生成化合物X(![]() ),
), 在Cu或Ag催化加热条件下,与O2发生氧化反应生成化合物Y(
在Cu或Ag催化加热条件下,与O2发生氧化反应生成化合物Y(![]() ),X与Y再发生反应生成
),X与Y再发生反应生成![]() 。
。


科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如下图,则此有机物可发生的反应类型有( )

①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化。
A. ①②③⑤⑥B. ②③④⑤⑥
C. ①②③④⑤D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
(1)高铁电池的负极材料是___。
(2)放电时,正极发生__(填“氧化”或“还原”)反应;负极的电极反应式为__。
(3)放电时,__(填“正”或“负”)极附近溶液的碱性增强。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置测定中和热的实验步骤如下:
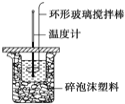
①用量筒量取50mL 0.50mol·L1盐酸倒入小烧杯中,测出盐酸的温度,然后把温度计上的酸用水冲洗干净;②用另一量筒量取50mL 0.55mol·L1 NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:
(1)大小烧杯间填满碎泡沫塑料的作用是:__________________________________。
(2)使盐酸与NaOH溶液混合均匀的正确操作是 ______ (填序号)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(3)大烧杯上如不盖硬纸板,求得的中和热数值将__________(填“偏大”“偏小”或“无影响”)。
(4)假设盐酸和氢氧化钠溶液的密度都是1g·cm3,又知中和反应后生成溶液的比热容c=4.18J·g1·℃1。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH= ______(结果保留一位小数)。
(5)______(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是 __
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Y具有抗菌、消炎作用,可由X制得。
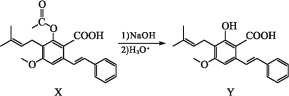
下列有关化合物X、Y的说法正确的是( )
A.1 mol X最多能与2mol NaOH反应
B.Y与羧酸发生酯化反应可得到X
C.X、Y均不能与酸性KMnO4溶液反应
D.室温下X、Y分别与足量Br2发生反应,且消耗Br2的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3CH2OH和 ![]() 互为同分异构体,将两种物质分别放在下列检测仪上进行检测,显示出的信号完全相同的是
互为同分异构体,将两种物质分别放在下列检测仪上进行检测,显示出的信号完全相同的是
A.李比希元素分析仪B.红外光谱仪C.核磁共振仪D.质谱仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数,下列说法正确的是
A.用氢氧燃料电池电解饱和食盐水得到 0.4mol NaOH,在燃料电池的负极上消耗氧气分子数为 0.1 NA
B.2 mol H3O+中含有的电子数为 20 NA
C.密闭容器中 1 mol N2(g)与 3 mol H2 (g)反应制备氨气,形成 6 NA 个 N-H 键
D.32 g N2H4中含有的共用电子对数为6 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在金属或非金属底物材料上,用NaBH4进行“化学镀”镀镍,可以得到坚硬、耐腐蚀的保护层(3Ni3B+Ni),反应的离子方程式为:
20Ni2++16BH4-+34OH-+6H2O===2(3 Ni3B+ Ni)+10B(OH)4-+35H2![]()
(1)Ni2+基态核外电子排布式为________。
(2)与BH4-互为等电子体的一种分子为______________![]() 填化学式
填化学式![]() 。
。
(3)B(OH)4-中硼原子轨道的杂化类型是________;1mol B(OH)4-含有σ键的数目为________mol。
(4)Ni的晶胞结构如图所示,镍晶体中每个镍原子周围距离最近的镍原子数目为________。
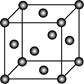
(5)NiCl2![]() 6H2O在SOCl2气流中加热时,生成NiCl2和两种酸性气体。写出该反应的化学方程式:__________________。
6H2O在SOCl2气流中加热时,生成NiCl2和两种酸性气体。写出该反应的化学方程式:__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com