
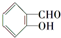
 中含有苯环的所有同分异构体
中含有苯环的所有同分异构体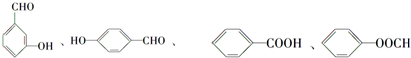
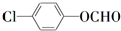 (写结构简式).
(写结构简式).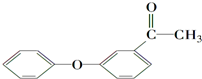 的一种同分异构体满足下列条件:
的一种同分异构体满足下列条件: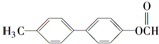 (写出一个就可以)
(写出一个就可以)分析 (1)根据官能团位置异构以及官能团异构来解答;
(2)C7H5O2Cl的同分异构体中含有苯环且Cl直接和苯环相接能发生银镜反应,说明分子中含有苯环、氯原子、醛基、羟基或酯基(甲酸某酯),可以看成苯环的二元取代产物或三元取代产物,有2个取代基时,有邻、间、对三不同结构;
根据核磁共振氢谱有三种不同化学环境的氢,说明有3种氢原子,峰面积之比等于个数之比以及含有醛基、羟基或酯基(甲酸某酯)来解答.
(3)根据能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应,说明含有酯基,且水解后得到酚羟基以及分子中等效氢的判断来解答;
(4)有机物X的分子式为C4H6O5,不饱和度为2,在有浓H2SO4和加热条件下,X与醇或羧酸均反应生成有香味的产物,说明该有机物分子中含有羧基和羟基;X在一定条件下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应,说明分子中羟基邻位碳上有氢原子;1molX与足量金属钠反应产生1.5mol气体,结合不饱和度以及氧原子守恒可知有机物分子中含有2个羧基和1个羟基,据此解答.
解答 解:(1) 中醛基和羟基可以处于间位、对位,当然还可以形成其他官能团羧基、酯基,所以含有苯环的所有同分异构体为:
中醛基和羟基可以处于间位、对位,当然还可以形成其他官能团羧基、酯基,所以含有苯环的所有同分异构体为: ;
;
故答案为: ;
;
(2)C7H5O2Cl的同分异构体中含有苯环且Cl直接和苯环相接能发生银镜反应,说明分子中含有苯环、氯原子、醛基、羟基或酯基(甲酸某酯),当分子中含有氯原子,酯基(甲酸某酯),有2个取代基时,有邻、间、对三不同结构,所以有3种结构;
当分子中含有氯原子,醛基、羟基,先考虑有2个取代基时,有邻、间、对三不同结构,所以有3种结构: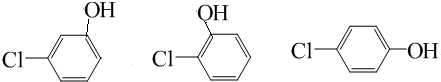 ,
,
再用醛基取代1个氢原子,其结构分别有:4种,4种,2种,共10种;
所以符合条件的共有13种;
某物质的分子式为C7H5O2Cl,其中核磁共振氢谱有三种不同化学环境的氢,且峰面积之比为2:2:1,含有含有醛基、羟基或酯基(甲酸某酯)的结构简式为: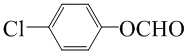 ;
;
故答案为:13; ;
;
(3)能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应,说明含有酯基,且水解后得到酚羟基,分子中有6种不同化学环境的氢,且分子中含有两个苯环,则该化合物的同分异构体的结构简式可能为: ;
;
故答案为: ;
;
(4)有机物X的分子式为C4H6O5,不饱和度为2,在有浓H2SO4和加热条件下,X与醇或羧酸均反应生成有香味的产物,说明该有机物分子中含有羧基和羟基;X在一定条件下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应,说明分子中羟基邻位碳上有氢原子;1molX与足量金属钠反应产生1.5mol气体,结合不饱和度以及氧原子守恒可知有机物分子中含有2个羧基和1个羟基,X 可能的结构简式:HOOCCH(OH)CH2COOH、(HOOC)2C(OH)CH3;
故答案为:HOOCCH(OH)CH2COOH、(HOOC)2C(OH)CH3.
点评 本题考查了有机物分子式、同分异构体的确定、结构简式的推断,注意核磁共振氢谱、官能团性质的运用,难度中等.


科目:高中化学 来源: 题型:解答题
| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴等浓度 FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡;试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生. |
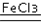 2H2O+O2↑.
2H2O+O2↑.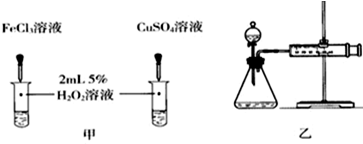
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
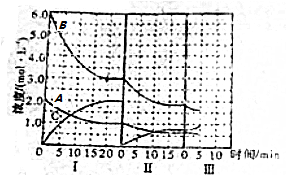
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na2O2+2H2O═4NaOH+O2↑ | B. | Mg3Cl2+2NaOH═Mg(OH)2↓+2NaCl | ||
| C. | 2NaOH+Cl2═NaOCl+H2O | D. | NH4Cl+NaO═NaCl+NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | 已知NH4F水溶液中含有HF分子,因此NH4F溶液不能存放于玻璃试剂瓶中 | |
| C. | 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 | |
| D. | 两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1=10c2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S(g)+O2(g)=SO2(g)放出热量大于297.23kJ | |
| B. | S(g)+O2(g)=SO2(g)放出热量小于297.23kJ | |
| C. | △H=-297.23kJ•mol-1表示固体S的燃烧热 | |
| D. | 形成1molSO2化学键释放的总能量大于断裂1molS(s)和1molO2(g)化学键吸收的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯原子的结构示意图为  | |
| B. | 质量数为37的氯原子${\;}_{17}^{37}$Cl | |
| C. | 氯化镁的电子式:Mg2+[Cl]2 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
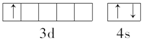 ,该元素基态原子结构示意图
,该元素基态原子结构示意图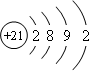 .该元素的名称为钪,形成的单质为金属晶体.
.该元素的名称为钪,形成的单质为金属晶体. 中心原子的杂化方式为
中心原子的杂化方式为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com