
取硝酸铜和铜粉的混合物,加热使其在空气中充分反应,反应前后质量不变, 则原混合物中含铜粉的质量分数是
[ ]
A. 74.6% B. 30.3% C. 69.7% D. 25.4%
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案科目:高中化学 来源: 题型:
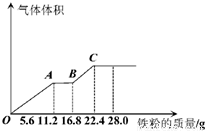
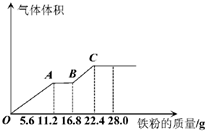 常温下,某200mL稀硫酸和稀硝酸的混合溶液最多能溶解19.2g铜粉(已知硝酸只被还原为NO气体),若再取等体积的该混合酸向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列有关分析错误的是( )
常温下,某200mL稀硫酸和稀硝酸的混合溶液最多能溶解19.2g铜粉(已知硝酸只被还原为NO气体),若再取等体积的该混合酸向其中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列有关分析错误的是( )查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:038
有一硫酸和硝酸的混合溶液,取出其中10 mL,加入足量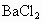 溶液,过滤、洗涤、烘干后得到9.32 g沉淀;滤液跟4 mol/L几的NaOH溶液反应,用去35 mL碱液时恰好完全中和.
溶液,过滤、洗涤、烘干后得到9.32 g沉淀;滤液跟4 mol/L几的NaOH溶液反应,用去35 mL碱液时恰好完全中和.
(1)求混合溶液中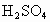 和
和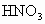 的物质的量浓度.
的物质的量浓度.
(2)另取10 mL原混合酸溶液,加入3.2 g铜粉共热,在标准状况下能生成多少毫升气体?
查看答案和解析>>
科目:高中化学 来源: 题型:058
有一硫酸和硝酸的混合溶液,取出其中10 mL,加入足量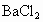 溶液,过滤、洗涤、烘干后得到9.32 g沉淀;滤液跟4 mol/L几的NaOH溶液反应,用去35 mL碱液时恰好完全中和.
溶液,过滤、洗涤、烘干后得到9.32 g沉淀;滤液跟4 mol/L几的NaOH溶液反应,用去35 mL碱液时恰好完全中和.
(1)求混合溶液中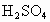 和
和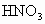 的物质的量浓度.
的物质的量浓度.
(2)另取10 mL原混合酸溶液,加入3.2 g铜粉共热,在标准状况下能生成多少毫升气体?
查看答案和解析>>
科目:高中化学 来源:2013-2014学年安徽省蚌埠市三县联谊校高三第二次联考理综化学试卷(解析版) 题型:实验题
某研究性学习小组的同学为验证浓硫酸与铜能反应而稀硫酸不能,设计了如图所示装置进行探究:将6.4 g 铜片和含0.2 moL溶质的18.4 mol/L浓硫酸放在圆底烧瓶中共热,直到无气体生成为止。(假定在此过程溶液体积不变)

(1)甲同学认为要证实上述结论,还应进行稀硫酸与铜片混合加热实验,你认为有无必要,并说明理由:________________
(2)下列试剂中能够用来进一步证明反应结束后的烧瓶中确有余酸的是:_____
A.铁粉 ?????? B.钠 ???? ?? C.氯化钡溶液 ???????? D.银粉
(3)为定量测定余酸的物质的量浓度,甲、乙两位同学进行了如下设计:
Ⅰ甲同学设想:在A装置增加一个导管通氮气驱赶气体(假定生成的气体全部逸出),先测定生成的SO2的量,然后计算剩余硫酸的浓度。他设计了如下二种方案来测定SO2的量:
方案① 将产生的气体缓缓通入足量用稀硫酸酸化的KMnO4溶液,再加入足量BaCl2溶液,过滤、洗涤、干燥、称量沉淀。
方案② 将气体缓缓通入足量硝酸钡溶液中,然后过滤、洗涤、干燥、称量沉淀。
经仔细分析后,发现有不合理之处,请填写下表(可以不填满):
序号 | 不合理的原因 | 误差 (偏低或偏高) | 改变措施 |
方案① |
|
|
|
方案② |
|
|
|
Ⅱ乙学生设计的方案是:分离出反应后的溶液并加蒸馏水稀释至1000 mL,取20.00 mL于锥形瓶中,滴入2~3滴酚酞指示剂,用标准NaOH溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),这种方法能否求出余酸的浓度,理由是_______________________________________。
(4)请再设计其他可行的实验方案,来测定余酸的物质的量浓度,简要写出操作步骤及需要测定的数据(不必计算,不必写操作细节)_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山东省聊城市临清市四校联考高三(上)期中化学试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com