
| A. | Cl-、Na+、SO42-、Al3+ | B. | NH4+、HCO3-、Cl-、K+ | ||
| C. | K+、Ba2+、Cl-、SO42- | D. | Fe2+、Mg2+、NO3-、Cl- |
分析 溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,强酸性溶液中存在大量氢离子,
A.四种离子之间不反应,都不与氢离子反应,且为无色溶液;
B.碳酸氢根离子与氢离子反应;
C.钡离子与硫酸根离子反应生成硫酸钡沉淀;
D.亚铁离子为有色离子,酸性条件下硝酸根离子能够氧化亚铁离子.
解答 解:无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,强酸性溶液中存在大量氢离子,
A.Cl-、Na+、SO42-、Al3+之间不反应,都为无色离子,都不与氢离子反应,在溶液中能够大量共存,故A正确;
B.HCO3-与氢离子反应,在溶液中不能大量共存,故B错误;
C.Ba2+、SO42-之间反应生成难溶物硫酸钡,在溶液中不能大量共存,故C错误;
D.Fe2+为有色离子,且酸性条件下Fe2+、NO3-发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;试题侧重对学生基础知识的训练和检验,有利于学生灵活运用基础知识解决实际问题的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 醋酸和氢氧化钠溶液 | B. | 氢氧化镁和硝酸 | ||
| C. | 氢氧化钠溶液和稀硫酸 | D. | 氢氧化钡和稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XeF4分子具有非常好的热稳定性 | |
| B. | XeF4分子中Xe的化合价为0价 | |
| C. | 氧化剂和还原剂的物质的量之比为2:3 | |
| D. | 每生成4molXe转移16mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
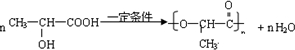
 是人体生理活动的一种代谢产物.以下是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物.请回答相关问题:
是人体生理活动的一种代谢产物.以下是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物.请回答相关问题:

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
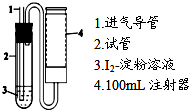 二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:
二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、H+、SO32-、H2O2 | B. | Al3+、Mg2+、OH-、CO32- | ||
| C. | K+、OH-、Cl-、NH3•H2O | D. | Ba2+、Fe3+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制氢气,为了加快反应速率,可向稀 H2SO4 中滴加少量 Cu(NO3)2 溶液 | |
| B. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变升高温度,平衡时氢气转化率增大 | |
| C. | 吸热反应“TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反 应的△S<0 | |
| D. | 为处理锅炉水垢中的 CaSO4,可先用饱和 Na2CO3 溶液浸泡,再加盐酸溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 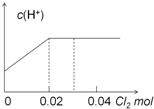 | B. |  | ||
| C. |  | D. | 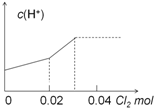 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{8b-3a}{2V}$mol•L-1 | B. | $\frac{8b-3a}{V}$mol•L-1 | C. | $\frac{a-2b}{V}$mol•L-1 | D. | $\frac{a-2b}{2V}$mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com