
| ��Ӧԭ�� | ʵ��װ�� | ʵ�鲽�� |
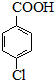
��1��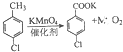 ��2�� 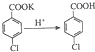 | 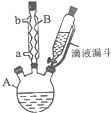 | ���ڹ��Ϊ250mL������A�м���һ�����Ĵ������������л��ܼ���������KMnO4��100mLˮ�� �ڰ�װ���������ڵ�Һ©���м���6.00mL���ȼױ������¶�Ϊ93������ʱ����ε�����ȼױ��� �ۿ����¶���93�����ң���Ӧ2h�����ȹ��ˣ�����������ˮϴ�ӣ�ʹϴ��Һ����Һ�ϲ�������ϡ�����ữ������Ũ������ȴ�� ���ٴι��ˣ�����������ˮ����ϴ�ӣ������Ƶ�������Ϊ7.19g |
| ��Է������� | �۵�/�� | �е�/�� | �ܶ�/g•cm-3 | ��ɫ | ˮ���� | |
| ���ȼױ� | 126.5 | 7.5 | 162 | 1.07 | ��ɫ | ���� |
| ���ȱ����� | 156.5 | 243 | 275 | 1.54 | ��ɫ | �� |
| ���ȱ������ | ���ڿ������� | |||||
���� һ�����Ķ��ȼױ�������KMnO4��93�淴Ӧһ��ʱ���ֹͣ��Ӧ���ɶ��ȱ�����غͶ������̣��������̲�����ˮ������ϡ�����ữ�����ɶ��ȱ����ᣬ���ȱ��������ڿ������Σ�����Ũ������ȴ�ᾧ�����ˣ�ϴ�������ö��ȱ����ᣮ
��1������������ͼ���жϣ�
��2��������Ӧ��������ͨˮ��
��3����ȡ6��OOmL���ȼױ��������ȡ������ȿ�֪Ӧѡ��ζ��ܣ��Ҷ��ȼױ�����ʴ��Ƥ�ܣ�
��4�������¶���93�����ң�����ˮ�ķе㣬���Բ�ȡˮԡ���ȣ�
��5���������̲�����ˮ�����˿ɳ�ȥ�����ȱ��������ϡ���ᷴӦ���ɶ��ȱ����ᣬ���ȱ���������ˮ���ǰ�ɫ������
��6����ȥ���ȱ��������Ŀ��������ʲ�������С���ȱ��������ģ�
��7�����ݶ��ȼױ�����������ȱ���������۲���������=$\frac{ʵ�ʲ���}{���۲���}$��100%��
��� �⣺��1����������ͼ�ο�֪��BΪ�����ܣ�
�ʴ�Ϊ�������ܣ�
��2��������Ӧ����a��ˮb��ˮ��ʹˮ���������ֽӴ���
�ʴ�Ϊ��a��
��3����ȡ6��OOmL���ȼױ��������ȡ������ȿ�֪Ӧѡ��ζ��ܣ����ȼױ���һ���������л��ܼ����Լ�ʽ�ζ���������Ʒ�����Ե��ܽⸯʴ���ã���ѡ25mL��ʽ�ζ��ܣ�
�ʴ�Ϊ��C��
��4�������¶���93�����ң�����ˮ�ķе㣬���Բ�ȡˮԡ���ȣ�
�ʴ�Ϊ��ˮԡ���ȣ�
��5�����ȼױ�������KMnO4��Ӧ���ɶ��ȱ�����غͶ������̣��������̲�����ˮ������۹��˵õ�����MnO2������������ˮϴ�ӣ��ɼ�С���ȱ�����ص���ģ���Һ�м���ϡ�����ữ�����ȱ��������ϡ���ᷴӦ���ɶ��ȱ����ᣬ���ȱ���������ˮ���ǰ�ɫ�������ɹ۲쵽��ʵ�������Dz�����ɫ������
�ʴ�Ϊ��MnO2����С���ȱ�����ص���ģ�������ɫ������
��6�����ȱ���������ˮ����ˮϴ�ӿ���������ȱ�������ܽ��ʹ����ģ�����ˮ����ϴ�Ӽȿɳ�ȥ���ȱ��������Ŀ��������ʻ��ܼ�С���ȱ��������ģ�
�ʴ�Ϊ���ɳ�ȥ���ȱ��������Ŀ����������Ҿ�����С���ȱ��������ģ�
��7�����ȼױ�������Ϊ��6ml��1.07g•cm-3=6.42g���� ��
�� ����֪���ȱ���������۲���Ϊ$\frac{6.42g}{126.5g/mol}$��156.5g��
����֪���ȱ���������۲���Ϊ$\frac{6.42g}{126.5g/mol}$��156.5g��
����ȱ�����IJ���Ϊ��[7.19g�£�$\frac{6.42g}{126.5g/mol}$��156.5g��]��100%��90.5%��
���� ���⿼���л�����Ʊ�ʵ�飬Ϊ�߿����������ͣ�ע����պϳ������еķ�Ӧ��������֪��Ϣ���ƶϸ����ʣ���Ϥ�л���Ľṹ�����ʼ��ɽ����Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | �۸�/Ԫ•��-1 |
| ƯҺ����25.2%NaClO�� | 450 |
| ˫��ˮ����30%H2O2�� | 2400 |
| �ռ��98%NaOH�� | 2100 |
| �����99.5%Na2CO3�� | 600 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Һ�����ڻ���������ɱ�� | |
| B�� | �����Ѿ�Ӫ���ḻ���������ǡ�ά����C�ȣ������������Ķ����������ö�������ԭ�ԣ���ֹ�����Ѿ���ijӪ���ɷֱ����� | |
| C�� | ij��ˮ����һ��ʱ���pH��4.68��Ϊ4.28����Ϊˮ�������ᱻ�������������������� | |
| D�� | ҽ���Ͽ������ᱵ��X�����ӳ�θ���ڷ�ҩ������Ϊ���ᱵ������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
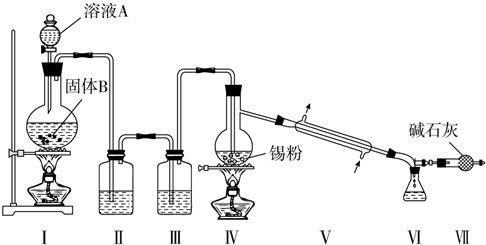
 A��B��C��D��E��F��G����ǰ������Ԫ����ԭ��������������A��������ۺ�����۵ľ���ֵ��ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�F�Ļ�̬ԭ�ӵ�3d�����������4s��������4����G2+��3d�����9�����ӣ���ش��������⣺
A��B��C��D��E��F��G����ǰ������Ԫ����ԭ��������������A��������ۺ�����۵ľ���ֵ��ȣ�B�Ļ�̬ԭ����3����ͬ���ܼ��Ҹ��ܼ��е�������ȣ�D�Ļ�̬ԭ����B�Ļ�̬ԭ�ӵ�δ�ɶԵ�����Ŀ��ͬ��E�Ļ�̬ԭ��s�ܼ��ĵ���������p�ܼ��ĵ�������ȣ�F�Ļ�̬ԭ�ӵ�3d�����������4s��������4����G2+��3d�����9�����ӣ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
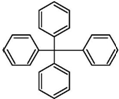 ��������е�4����ԭ��ȫ��������ȡ�����������ʵķ��ӽṹ��ͼ��ʾ���Ը����ʵ���������ȷ���ǣ�������
��������е�4����ԭ��ȫ��������ȡ�����������ʵķ��ӽṹ��ͼ��ʾ���Ը����ʵ���������ȷ���ǣ�������| A�� | �����ʽΪC25H20 | |
| B�� | �����ڵ�����̼ԭ�Ӳ����ܹ�ƽ�� | |
| C�� | �����ʹ����¿ɺ�����������Ӧ | |
| D�� | ��������Fe�۴��¿ɺ�Һ�巢����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
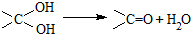 �����
���л���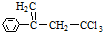 ��ѡ�������������Գ��ݼ����׳ư�ϩ����Ҫ����ˮ��������ݣ������йظ��л����˵��������ǣ�������
��ѡ�������������Գ��ݼ����׳ư�ϩ����Ҫ����ˮ��������ݣ������йظ��л����˵��������ǣ�������| A�� | ��ʹ���Ը��������Һ��ɫ | |
| B�� | ���� ��Cl2�ڹ���������ͨ��ȡ����Ӧ��ýϴ��ĸ����� ��Cl2�ڹ���������ͨ��ȡ����Ӧ��ýϴ��ĸ����� | |
| C�� | �ڼ��������³��ˮ�⣬������������ | |
| D�� | ��һ�������¿ɷ����ۺϷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼ��һ���绯ѧ����ʾ��ͼ��
��ͼ��һ���绯ѧ����ʾ��ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
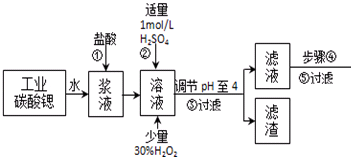
| �������� | Fe��OH��3 | Fe��OH��2 |
| ��ʼ������pH | 1.5 | 6.5 |
| ������ȫ��pH | 3.7 | 9.7 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com