
分析 因为该反应是可逆反应,反应物不能完全转化为生成物,该方程式表示为转化1mol氮气放出92.2kJ热量,在该条件下氮气的转化率仅为10%,则投入的氮气物质的量>$\frac{反应的氮气}{转化率}$.
解答 解:因为该反应是可逆反应,反应物不能完全转化为生成物,该方程式表示为转化1mol氮气放出92.2kJ热量,在该条件下氮气的转化率仅为10%则投入的氮气物质的量>$\frac{反应的氮气}{转化率}$=$\frac{1mol}{10%}$=10mol,
故答案为:大于10.
点评 本题考查物质的量的有关计算,为高频考点,侧重考查学生分析计算能力,明确转化率与参加反应的关系是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在偏二甲肼与四氧化二氮的反应中,N2O4是氧化剂 | |
| B. | 两物质反应时,生成的无毒气体为CO2、N2、和H2O | |
| C. | 偏二甲肼中N元素的化合价均为-2价 | |
| D. | 偏二甲肼的同分异构体中,含碳碳单键的化合物只有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
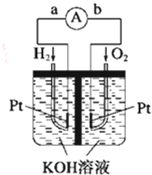 燃料电池是符合绿色化学理念的新型发电装置.如图为氢氧燃料电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
燃料电池是符合绿色化学理念的新型发电装置.如图为氢氧燃料电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 日本的水俣病是由重金属镉污染引起的 | |
| B. | 垃圾处理要遵循无害化、减量化和资源化的原则 | |
| C. | 水体的富营养化是由于水体中植物营养物质过多蓄积而引起的污染 | |
| D. | 污水处理中混凝法、中和法、沉淀法、氧化还原法等都是化学方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
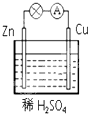 在如图所示的锌铜原电池中,Zn作原电池的负极,电极上发生的是氧化反应(填“氧化”或“还原”),该电极反应式为Zn-2e-=Zn2+,观察到的现象为锌片溶解;Cu作原电池的正 极,电极上发生的是还原反应(填“氧化”或“还原”),该电极反应式为2H++2e-=H2↑,观察到的现象为铜片上有气泡产生.
在如图所示的锌铜原电池中,Zn作原电池的负极,电极上发生的是氧化反应(填“氧化”或“还原”),该电极反应式为Zn-2e-=Zn2+,观察到的现象为锌片溶解;Cu作原电池的正 极,电极上发生的是还原反应(填“氧化”或“还原”),该电极反应式为2H++2e-=H2↑,观察到的现象为铜片上有气泡产生.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量为18g | B. | 含有NA个氧原子 | ||
| C. | 标准状况下体积约为22.4L | D. | 含有NA个水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O=CaSO4↓+H++Cl-+HClO | |
| B. | 向FeCl2溶液加入足量NaClO溶液:6Fe2++3ClO-+3H2O=2Fe(OH)3↓+4Fe3++3Cl- | |
| C. | NH4HCO3溶液和少量的NaOH溶液混合:HCO3-+OH-═CO32-+H2O | |
| D. | 向Fe(NO3)3溶液中加入足量的HI溶液:2Fe3++2I-=2Fe2++I2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com