
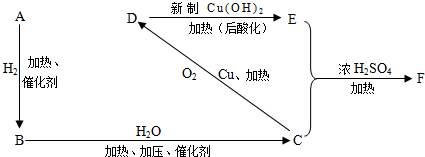
·ÖĪö AµÄĆÜ¶Č£ØŌŚ±ź×¼×“æöĻĀ£©ŹĒĒāĘųµÄ13±¶£¬ĖµĆ÷AµÄ·Ö×ÓĮæŹĒ26£¬ĖłŅŌAŹĒŅŅČ²£¬ŅŅČ²æÉŅŌŗĶĒāĘų·¢Éś¼Ó³É·“Ó¦£¬Éś³ÉŅŅĻ©£¬ĖłŅŌBŹĒŅŅĻ©£¬ŅŅĻ©æÉŅŌŗĶĖ®·¢Éś¼Ó³É·“Ӧɜ³ÉŅŅ“¼£¬¼“CŹĒŅŅ“¼£¬ŅŅ“¼“ß»ÆŃõ»ÆæÉŅŌµĆµ½ŅŅČ©£¬¼“DĪŖŅŅČ©£¬ŅŅČ©Ņ×±»Ńõ»ÆĪŖŅŅĖį£¬¼“EŹĒŅŅĖį£¬ŅŅĖįŗĶŅŅ“¼Ö®¼äæÉŅŌÉś³ÉŅŅĖįŅŅõ„£¬¼“FŹĒŅŅĖįŅŅõ„£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗAµÄĆÜ¶Č£ØŌŚ±ź×¼×“æöĻĀ£©ŹĒĒāĘųµÄ13±¶£¬ĖµĆ÷AµÄ·Ö×ÓĮæŹĒ26£¬ĖłŅŌAŹĒŅŅČ²£¬ŅŅČ²æÉŅŌŗĶĒāĘų·¢Éś¼Ó³É·“Ó¦£¬Éś³ÉŅŅĻ©£¬ĖłŅŌBŹĒŅŅĻ©£¬ŅŅĻ©æÉŅŌŗĶĖ®·¢Éś¼Ó³É·“Ӧɜ³ÉŅŅ“¼£¬¼“CŹĒŅŅ“¼£¬ŅŅ“¼“ß»ÆŃõ»ÆæÉŅŌµĆµ½ŅŅČ©£¬¼“DĪŖŅŅČ©£¬ŅŅČ©Ņ×±»Ńõ»ÆĪŖŅŅĖį£¬¼“EŹĒŅŅĖį£¬ŅŅĖįŗĶŅŅ“¼Ö®¼äæÉŅŌÉś³ÉŅŅĖįŅŅõ„£¬¼“FŹĒŅŅĖįŅŅõ„£®
£Ø1£©ÓÉŅŌÉĻ·ÖĪöæÉÖŖAĪŖCH”ŌCH£¬DĪŖŅŅČ©£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖČ©»ł£¬¹Ź“š°øĪŖ£ŗCH”ŌCH£»Č©»ł£»
£Ø2£©ÓÉŅŌÉĻ·ÖĪöæÉÖŖEĪŖCH3COOH£¬FĪŖCH3COOCH2CH3£¬¹Ź“š°øĪŖ£ŗCH3COOH£»CH3COOCH2CH3£»
£Ø3£©ŅŅĖįŗĶŅŅ“¼æÉŅŌ·¢Éśõ„»Æ·“Ó¦£¬Éś³Éõ„£¬·½³ĢŹ½ĪŖCH3CH2OH+CH3COOH$?_{”÷}^{ÅØĮņĖį}$CH3COOCH2CH3+H2O£¬D”śE·“Ó¦ĪŖCH3CHO+2Cu£ØOH£©2$\stackrel{”÷}{”ś}$CH3COOH+Cu2O”ż+2H2O£¬
¹Ź“š°øĪŖ£ŗCH3CH2OH+CH3COOH$?_{”÷}^{ÅØĮņĖį}$CH3COOCH2CH3+H2O£»CH3CHO+2Cu£ØOH£©2$\stackrel{”÷}{”ś}$CH3COOH+Cu2O”ż+2H2O£»
£Ø4£©C”śDµÄ·“Ó¦ĄąŠĶŹōÓŚŃõ»Æ·“Ó¦£®C+E”śFµÄ·“Ó¦ĄąŠĶŹōÓŚõ„»Æ·“Ó¦£¬¹Ź“š°øĪŖ£ŗŃõ»Æ£»õ„»Æ£»
£Ø5£©FĪŖCH3COOCH2CH3£¬¶ŌÓ¦µÄĶ¬·ÖŅģ¹¹ĢåÄÜÓėNaHCO3·“Ó¦²śÉśĘųĢ壬ĖµĆ÷ŗ¬ÓŠōČ»ł£¬Ōņ¶ŌÓ¦µÄĶ¬·ÖŅģ¹¹ĢåÓŠCH3CH2CH2COOH”¢CH3CH£ØCH3£©COOH£¬¹²2ÖÖ£¬
¹Ź“š°øĪŖ£ŗ2£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕ¹ŁÄÜĶÅÓėŠŌÖŹµÄ¹ŲĻµ”¢ÕĘĪÕČ²Ģž”¢Ļ©Ģž”¢“¼”¢Č©”¢ōČĖįÖ®¼äµÄ×Ŗ»Æ¹ŲĻµŹĒ½ā“šµÄ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
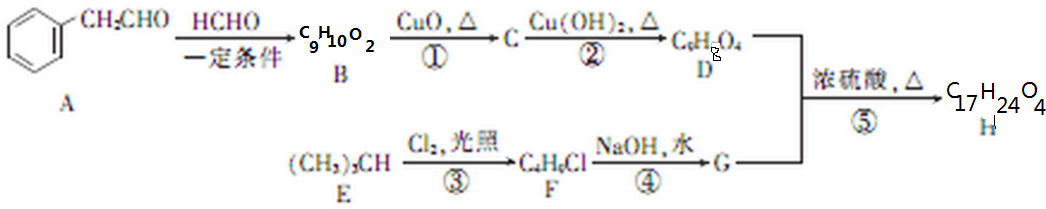
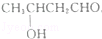
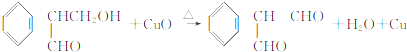
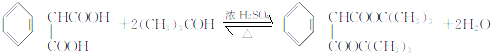
 £Ø²»æ¼ĀĒĮ¢ĢåŅģ¹¹£©£æ
£Ø²»æ¼ĀĒĮ¢ĢåŅģ¹¹£©£æ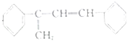 µÄŗĻ³ÉĀ·Ļߣ®
µÄŗĻ³ÉĀ·Ļߣ®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | N2”¢H2O”¢NO | B£® | NH3”¢CO2”¢NO | C£® | NH3”¢O2”¢NO | D£® | H2O”¢NO2”¢CO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH4 | B£® | BF3 | C£® | CO2 | D£® | N2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 ÖÖ | B£® | 2ÖÖ | C£® | 3ÖÖ | D£® | 4ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
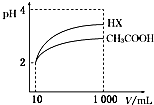 25”ꏱ£¬ČżÖÖĖįµÄµēĄė³£ŹżĪŖ£ŗ
25”ꏱ£¬ČżÖÖĖįµÄµēĄė³£ŹżĪŖ£ŗ| »ÆѧŹ½ | CH3COOH | H2CO3 | HClO |
| µēĄėĘ½ŗā³£ŹżK | 1.8”Į10-5 | K1=4.3”Į10-7 K2=5.6”Į10-11 | 3.0”Į10-8 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com