
| A.复盐的溶解度一般比组成它的每一种盐都小 |
| B.合金的熔点一般比组成它的每一种金属都高 |
| C.用NaOH溶液和铝盐反应得不到Al(OH)3沉淀,因此一般用氨水与铝盐反应制备 Al(OH)3 |
| D.萃取剂选择的标准之一是不能与被萃取的物质反应,并且密度要比原溶剂大 |
科目:高中化学 来源:不详 题型:填空题

| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
| A.KMnO4 | B.Cl2 | C.MgO | D.CaO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.容器内气体压强保持不变 |
| B.容器内各物质的浓度不随时间变化 |
| C.当υ(H2,正)=0.3mol·L-1·min-1,υ(NH3,逆)=0.2mol·L-1·min-1时 |
| D.1个N≡N键断裂的同时,有3个H-H键形成 |
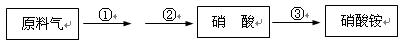
 4HNO3,原料气为氨气和空气的混合物。
4HNO3,原料气为氨气和空气的混合物。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
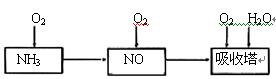
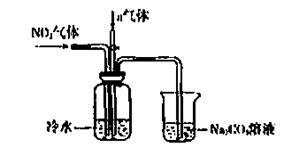
 (6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K= 。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为 。
(6)一定条件下,某密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.500mol/L,c(N2O4)=0.125mol/L。则2NO2(g) N2O4(g)的平衡常数K= 。若NO2起始浓度为2mol/L,相同条件下,NO2的最大转化率为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
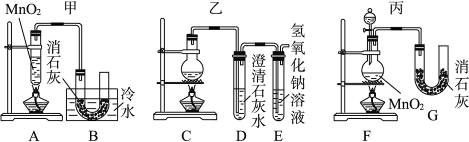
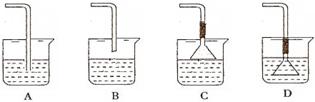
| | 优点 | 缺点 |
| ①甲装置 | | |
| ②乙装置 | | |
| ③丙装置 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
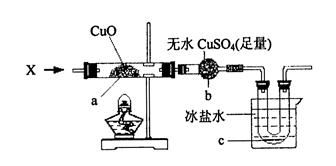
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.配制0.1 mol·L-1 100 mL的CuSO4溶液 |
| B.蒸发 |
| C.测定硫酸铜晶体中结晶水的含量 |
| D.萃取、分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com