
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。完成下列计算:
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠________ g。
(2)钠—钾合金可在核反应堆中用作热交换液。5.05 g钠—钾合金溶于200 mL水生成0.075 mol氢气。
①计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
②计算并确定该钠-钾合金的化学式。
(3)氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2―→2Al(OH)3↓+Na2CO3+H2O,己知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112 L(标准状 况下),计算生成的Al(OH)3和Na2CO3的物质的量之比。
况下),计算生成的Al(OH)3和Na2CO3的物质的量之比。
解析 (1)利用“N”守恒可知需m(NaN3)=(40.32 L/22.4 L·mol-1)×2/3×65 g·mol-1=78 g。
(2)①由反应方程式可知产生1 mol H2同时生成2 mol OH-,故c(OH-)=(0.075 mol×2)/0.2 L=0.75 mol·L-1;②设合金中Na、K的物质的量分别为a mol、b mol,然后利用质量守恒与得失电子守恒可得方程式:a+b=0.75×2和23a+39b=5.05,解之得a=0.050 mol、b=0.10 mol,故可得到合金的化学式为NaK2。
(3)若溶液中仅含NaAl(OH)4,利用方程式可知得到24 mol Al(OH)3的同时生成12 mol Na2CO3,而实际得到24 mol Al(OH)3与15 mol Na2CO3,说明溶液中含有NaOH, 且NaOH优先与CO2反应生成Na2CO3,利用Na守恒知溶液中n(NaOH)=(15-12) mol×2=6 mol,故通入112 L CO2(5 mol)先与N
且NaOH优先与CO2反应生成Na2CO3,利用Na守恒知溶液中n(NaOH)=(15-12) mol×2=6 mol,故通入112 L CO2(5 mol)先与N aOH作用消耗CO2 3 mol生成3 mol Na2CO3,然后2 mol
aOH作用消耗CO2 3 mol生成3 mol Na2CO3,然后2 mol  CO2与NaAl(OH)4作用得到4 mol Al(OH)3和2 mol Na2CO3,故生成n[Al(OH)3]∶n(Na2CO3)=4∶(3+2)=4∶5。
CO2与NaAl(OH)4作用得到4 mol Al(OH)3和2 mol Na2CO3,故生成n[Al(OH)3]∶n(Na2CO3)=4∶(3+2)=4∶5。
答案 (1)78 (2)①c(OH-)=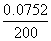 ×1 000=0.75(mol·L-1) ②设上述合金中含a mol Na、b mol K,a+b=0.75×2,23a+39b=5.05,a=0.050 mol,b=0.10 mol,该钠—钾合金化学式为NaK2 (3)溶液含NaOH,NaOH与CO2反应生成的Na2CO3:15-
×1 000=0.75(mol·L-1) ②设上述合金中含a mol Na、b mol K,a+b=0.75×2,23a+39b=5.05,a=0.050 mol,b=0.10 mol,该钠—钾合金化学式为NaK2 (3)溶液含NaOH,NaOH与CO2反应生成的Na2CO3:15-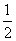 ×24=3(mol),112 L CO2的物质的量:112/22.4=5(mol),n[Al(OH)3]∶n(Na2CO3)=[(5-3)×2]∶5=4∶5
×24=3(mol),112 L CO2的物质的量:112/22.4=5(mol),n[Al(OH)3]∶n(Na2CO3)=[(5-3)×2]∶5=4∶5


科目:高中化学 来源: 题型:
热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本
结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca =CaCl2+Li2SO4+Pb。下列有关说法正确的是: (已知:Pb的原子量 207 ) ( )
A.正极反应式:Ca+2Cl- - 2e- =CaCl2
B.放电过程中,Li+ 向负极移动
C.每转移0.1mol电子,理论上生成20.7gPb
D.常温时,在正负极间接上电流表或检流计,指针不偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气(H2)、一氧化碳(CO)、辛烷(C8H18)、甲烷(CH4)的热化学方程式分别为:
H2(g)+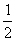 O2(g)====H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)====H2O(l) ΔH=-285.8 kJ·mol-1
CO(g)+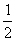 O2(g) ====CO2(g) ΔH=-283.0 kJ·mol-1
O2(g) ====CO2(g) ΔH=-283.0 kJ·mol-1
C8H18(l)+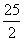 O2(g) ====8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
O2(g) ====8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
CH4(g)+2O2(g) ====CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
相同质量的H2、CO、C8H18、CH4完全燃烧时,放出热量最少的是( )
A.H2(g) B.CO(g) C.C8H18(l) D.CH4(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列做法正确的是
A.将浓硝酸保存在无色玻璃瓶中
B.金属钠和钾保存在煤油中
C.Na2CO3可以保存在玻璃塞的玻璃瓶中
D.NaOH固体放在滤纸上称量
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的NaHCO3和Na2CO3混合物,向其中加入500 mL HCl溶液后溶液呈中性,产生标况下CO2气体4.48 L,若将等量的NaHCO3和Na2CO3混合物加热后,产生气体(包括H2O)用碱石灰吸收,碱石灰增重4.65 g,则下列叙述正确的是
A.加热时生成的气体在标况下3.36 L
B.NaHCO3和Na2CO3混合物质量为17.9 g
C.加热时若用浓硫酸吸收气体则浓硫酸增重3.3 g
D.HCl溶液的浓度为0.6 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
医疗上的血液透析原理同胶体的渗析类似。透析时,病人的血液通过浸在透析液中的透析膜进行循环和透析。血液中,蛋白质和血细胞不能通过透析膜,血液中的毒性物质可以透过,由此可以判断( )
A.蛋白质、血细胞的粒子直径大于毒性物质的直径
B.蛋白质以分子形式存在,毒性物质以离子形式存在
C.蛋白质、血细胞不溶于水,毒性物质可溶于水
D.蛋白质、血细胞不能透过滤纸,毒性物质可以透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度、相同浓度下的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别为( )

A.NH4Cl (NH4)2SO4 CH3COONa
B.(NH4)2SO4 NH4Cl CH3COONa
C.(NH4)2SO4 NH4Cl NaOH
D.CH3COOH NH4Cl (NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.丙烯酸和油酸互为同系物 B.淀粉和纤维素互为同分异构体
C.CuSO4浓溶液能使蛋白质溶液发生盐析
D.葡萄糖和脂肪在一定条件下都能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组探究SO2气体还原Fe3+,他们使用的药品和装置如图所示:
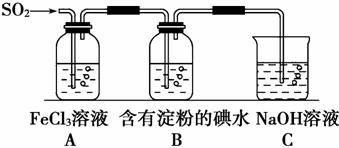
下列说法不合理的是
A.能表明I-的还原性弱于SO2的现象是B中蓝色溶液褪色
B.装置C的作用是吸收SO2尾气,防止污染空气
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的BaCl2,产生白色沉淀
D.为了验证A中发生了氧化还原反应,加入KMnO4溶液,紫红色褪去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com