
【题目】有关下列四个常用电化学装置的叙述正确的是( )
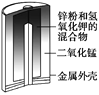
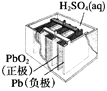
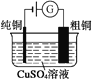
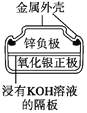
图1 碱性锌锰电池 图2 铅—硫酸蓄电池 图3 电解精炼铜 图4 银锌纽扣电池
A. 图1所示电池中,MnO2的作用是催化剂
B. 图2所示电池放电过程中,硫酸浓度不断增大
C. 图3所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图4所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
科目:高中化学 来源: 题型:
【题目】下列反应属于皂化反应的是( )
A.乙酸乙酯在碱性条件下的水解
B.硬脂酸甘油酯在酸性条件下的水解
C.软脂酸甘油酯在碱性条件下的水解
D.油酸甘油酯在酸性条件下的水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在80℃时,将0.40 mol的N2O4气体充入2 L已经抽成真空的固定容积的密闭容器中,发生反应N2O4(g)![]() 2NO2(g),隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2(g),隔一段时间对该容器内的物质进行分析,得到如下数据:
| 0 | 20 | 40 | 60 | 80 | 100 |
n(N2O4) | 0.40 | a | 0. 20 | c | d | e |
n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)计算20~40 s内用N2O4表示的平均反应速率为 ___________mol L-1·s-1
(2)计算在80℃时该反应的平衡常数K =____________(请注明单位)。
(3)反应进行至100s后将反应混合物的温度降低,混合气体的颜色________(填“变浅”“变深”或“不变)。
(4)要增大该反应的K值,可采取的措施有_________(填字母代号)
A.增大N2O4起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线_________。
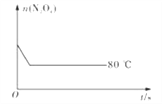
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向25mL18.4mol/LH2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量( )
A.小于0.23mol
B.等于0.23mol
C.0.23mol~0.46mol之间
D.等于0.46mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cu跟浓H2SO4反应,得到SO2的体积为22.4L(标准状况).把所得的CuSO4配制成500mL溶液.求:
(1)反应过程中转移电子的物质的量.
(2)所得溶液中溶质的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于油脂的叙述错误的一项是( )
A.从溴水中提取溴可用植物油作萃取剂
B.用热的纯碱溶液去油污效果更好
C.硬水使肥皂去污能力减弱是因为发生了沉淀反应
D.用热的纯碱溶液可区别植物油和矿物油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学方程式可简明地体现元素及其化合物的性质。已知:氧化还原反应:
2FeCl3+2HI===2FeCl2+I2+2HCl 2Co(OH)3+6HCl===2CoCl2+Cl2↑+6H2O
2Fe(OH)2+I2+2KOH===2Fe(OH)3+2KI 3I2+6KOH===5KI+KIO3+3H2O
复分解反应:
2HSCN+K2CO3===2KSCN+CO2↑+H2O KCN+CO2+H2O===HCN+KHCO3
热分解反应:
4NaClO![]() 3NaCl+NaClO4 NaClO4
3NaCl+NaClO4 NaClO4![]() NaCl+2O2↑
NaCl+2O2↑
下列说法不正确的是
A. 氧化性(酸性溶液):FeCl3>Co(OH)3>I2 B. 还原性(碱性溶液):Fe(OH)2>I2>KIO3
C. 热稳定性:NaCl>NaClO4>NaClO D. 酸性(水溶液):HSCN>H2CO3>HCN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的根本原因是
A. 元素原子的核外电子排布呈周期性变化
B. 元素的金属性和非金属性呈周期性变化
C. 元素的原子半径呈周期性变化
D. 元素化合价呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是
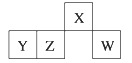
A. 原子半径:rW>rZ>rY>rX
B. 含Y元素的盐溶液一定显酸性
C. 最简单气态氢化物的热稳定性:X>W
D. Z的最高价氧化物的水化物难溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com