
【题目】已知c(NH4Cl)≤0.1 mol/L时,溶液pH>5.1。现用0.1 mol/L盐酸滴定10 mL 0.05 mol/L氨水,用甲基橙作指示剂,达到滴定终点,所用盐酸的体积为
A. 10 mL B. 5 mL C. 大于5 mL D. 小于5 mL
科目:高中化学 来源: 题型:
【题目】已知常温、常压下,饱和CO2溶液的pH为3.9,用标准浓度的盐酸来滴定锥形瓶中放置时间较长的氢氧化钠溶液,应选用的指示剂及滴定终点颜色变化的情况最好是( )
A.石蕊,由蓝变红 B.酚酞,红色褪去
C.甲基橙,由黄变橙 D.甲基橙,由橙变黄
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红磷(P)和Cl2发生反应生成PCl3和PCl5,反应过程和能量的关系如图所示,图中的ΔH表示生成1 mol产物的数据。可知PCl5分解生成PCl3和Cl2,该分解反应是可逆反应。下列说法正确的是( )
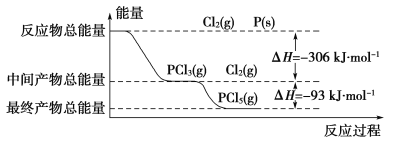
A.其他条件不变,升高温度有利于PCl5的生成
B.反应2P(s)+5Cl2(g)==2PCl5(g)对应的反应热 ΔH=-798 kJ·mol-1
C.P和Cl2反应生成PCl3的热化学方程式为:2P(s)+3Cl2(g)==2PCl3(g) ΔH=-306 kJ·mol-1
D.其他条件不变,对于2PCl5(g)==2P(s)+5Cl2(g) ΔH反应,增大压强,PCl5的转化率减小,ΔH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的能量变化与其他三项不相同的是( )
A. 铝粉与氧化铁的反应 B. 氯化铵与Ba(OH)2 ·8H2O的反应
C. 锌片与稀硫酸反应 D. 钠与冷水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取50.0mLNa2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66g,并有气体放出,试计算:
(1)原混合液中SO42-的物质的量浓度?Na+的物质的量浓度?
(2)产生的气体在标准状况下的体积升。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,能在溶液中大量共存的是( )
A. Ba2+、Na+、OH-、SO42- B. Na+、H+、NO3-、CO32-
C. Mg2+、SO42-、K+、Cl- D. K+、Cu2+、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
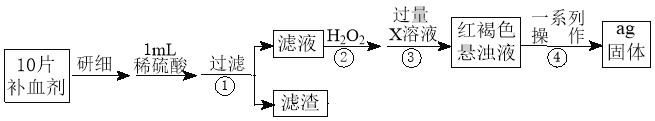
请回答下列问题:
(1) 向步骤①的滤液中滴加KSCN溶液后变为红色,则该滤液中含有 (填离子符号),检验滤液中还存在Fe2+的方法为 (说明试剂、现象)。
(2) 步骤②加入过量H2O2的目的是 。
(3) 步骤③中反应的离子方程式为 。
(4) 步骤④中一系列处理的操作步骤包括:过滤、 、灼烧、 、称量。
(5) 假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一无色透明的溶液做如下实验:
(1)取少量溶液滴加盐酸酸化的BaCl2溶液,有白色沉淀生成。
(2)另取部分溶液加入Na2O2,有无色无味气体放出且有白色沉淀生成,加入Na2O2的量与生成沉淀的量的关系如图所示:
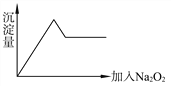
试问:
(1)Cu2+、NH4+、Al3+、Mg2+、Na+、Fe3+、CO32--、K+、SO42--等离子中一定存在的离子是_________________;可能存在的离子是_____________;一定不存在的离子是_____________________。
(2)上述溶液至少由___________________等物质混合成。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离的c(H+)=1×10-13 mol/L,该溶液可能是( )
①二氧化硫水溶液 ②氯化铵水溶液 ③硝酸钠水溶液 ④氢氧化钠水溶液
A. ①④ B. ①② C. ②③ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com