
 把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58 g白色沉淀生成,在所得的浑浊液中,逐滴加入0.5 mol/L盐酸,加入盐酸的体积(V)与生成沉淀的质量(W)关系如图所示:
把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58 g白色沉淀生成,在所得的浑浊液中,逐滴加入0.5 mol/L盐酸,加入盐酸的体积(V)与生成沉淀的质量(W)关系如图所示:| 0.035mol |
| 0.5mol/L |


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| pH | c(CrO42-) | c(HCrO4-) | c(Cr2O72-) | c(H2CrO4) |
| 4 | 0.0003 | 0.1030 | 0.4480 | 0 |
| 6 | 0.0319 | 0.0899 | 0.4370 | 0 |
| 7 | 0.2645 | 0.0860 | 0.3195 | 0 |
| 9 | 0.8960 | 0.0031 | 0.0004 | 0 |
| A、铬酸的第一步电离方程式为:H2CrO4=H++HCrO4- |
| B、该铬酸溶液的物质的量浓度约为1.00mol/L |
| C、pH越大,HCrO4-越容易电离出CrO42- |
| D、NaHCrO4溶液中:c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 浓H2SO4 |
| △ |
| CH3OH |
| 浓H2SO4 |

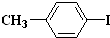 和
和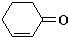 也可以发生类似反应①的反应,反应后有机产物的结构简式为
也可以发生类似反应①的反应,反应后有机产物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A、反应开始20s内二氧化氮的平均反应速率是0.001mol?L-1 |
| B、80s时混合气体的颜色与60s时颜色相同,比40s时的颜色深 |
| C、80s时向容器内加0.32molHe,同时将容器扩大为4L,则平衡不移动 |
| D、若起始投料为0.20molN2O4相同条件下达到平衡,则各组分的含量与原平衡相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某钠盐溶液含甲电离出的阴离子,则该溶液显碱性且能与酸反应 |
| B、乙与氧气的摩尔质量相同,则乙可能是N2H4或CH3OH |
| C、丙中含有第2周期ⅣA族的元素,则丙一定是甲烷的同系物 |
| D、丁和甲中各元素质量比相同,则丁中一定含有-1价的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
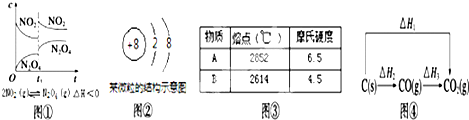
| A、图①t1时改变的条件可能是升高了温度或增大了压强 |
| B、图②该微粒仅为18O2-不能为16O2- |
| C、图③若A为CaO,则B可能为MgO |
| D、图④中的△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com