
【题目】下列关于胆矾(CuSO4·5H2O)的说法中错误的是
A. 它属于纯净物 B. 它属于硫酸盐
C. 它属于铜盐 D. 它属于混合物
科目:高中化学 来源: 题型:
【题目】将4molSO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2+O22SO3 测得平衡时SO3的浓度为0.5mol/L,求:
(1)平衡时各物质的浓度;
(2)平衡时SO2的转化率;
(3)该条件下的平衡常数K.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸是﹣种常见的有机酸,结构简式为 ![]() ,下列说法不正确的是( )
,下列说法不正确的是( )
A.苹果酸能使紫色的石蕊试液变红
B.苹果酸能发生酯化反应
C.![]() 与苹果酸是同一种物质
与苹果酸是同一种物质
D.1mol苹果酸在一定条件下可与2molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)①在淀粉碘化钾溶液中,滴加少量次氯酸钠溶液,溶液变蓝色,且反应后溶液显碱性,发生反应的离子方程式为 . ②在上述碘和淀粉形成的蓝色溶液中,滴加亚硫酸钠碱性溶液,发现蓝色逐渐消失,写出发生反应的离子方程式 .
③对比①和②实验所得的结果,将I2、ClO﹣、SO ![]() 按氧化性由强到弱的顺序排列为 .
按氧化性由强到弱的顺序排列为 .
(2)今有铁皮、铜片、酸、碱、盐溶液若干.设计实验证明以下事实,写出反应的化学方程式.①浓硫酸的氧化性比稀硫酸强: .
②氯化铁溶液中Fe3+的氧化性比硫酸铜溶液中的Cu2+强: .
③铁的还原性比铜强: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵俗名摩尔盐.化学式为x(NH4)2SO4yFeSO4zH2O,可用来净水或治疗缺铁性贫血等.某实验小组利用下面的方法来测定其组成.
①NH4+含量测定:称取9.8g硫酸亚铁铵晶体,加适量水溶解,注人如图所示的三颈瓶中,然后逐滴加人足量lO%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用lOOmL 1.0molL﹣1的盐酸标准溶液吸收.
蒸氨结束后取下接收瓶,用1.0molL﹣1NaOH标准溶液滴定剩余的HCl,到终点时消耗50mlNaOH溶液.
②Fe2+含量测定:向上述实验后的三颈瓶中加入过量的3%的双氧水,充分反应后过滤、洗涤、灼烧得到2.0g固体.
③结晶水含量测定:称取9.8g硫酸亚铁铵晶体,在质量为15g的坩埚中加热至200℃,恒温一段时间,置于空气中冷却,称量质量为22.3g;重复上述加热、冷却、称量过程,发现两次称量结果相同.回答下列问题: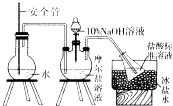
(1)装置中安全管的作用原理是 .
(2)冰盐水的作用是 .
(3)用NaOH标准溶液滴定剩余的HCl时,可使用的指示剂是 .
(4)测定Fe2+时.加人双氧水发生反应的化学方程式是 .
(5)如果在测定NH4+含量的过程中,亚铁元素部分被氧化,对Fe2+含量的测定(填“有”或“无”)影响.
(6)根据①、②的数据,该摩尔盐晶体中n(NH4+):n(Fe2+):n(SO42﹣ )= , z= .
(7)根据③的数据,发现结晶水含量测定结果偏低.从实验过程分析,可能原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期,世界范围内有成千上万个湖泊变为鱼类绝迹的死湖,数以千万公顷计的森林衰败枯萎,大片土地沙漠化…将这些现象与频繁降落的酸雨相联系,人们认为,酸雨是肇事主因.某研究小组研究某地硫酸酸雨的形成,有人提出以下猜想: 猜想一:SO2 ![]() SO3
SO3 ![]()
![]()
猜想二:S02 ![]()
![]()
![]()
![]()
猜想三:以上两过程同时存在
有关上述猜想,收集一定量该地区刚下的雨水进行实验,下列判断中错误的是( )
A.若猜想一或猜想三正确,则该雨水加入盐酸后,再加入BaCl2溶液,有白色沉淀生成
B.若存在猜想二的过程,则该雨水可能使品红褪色
C.若只存在猜想一的过程,则该雨水的pH随时间延长而增大
D.上述任意一个猜想正确,该地区雨水的pH均小于5.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为 ![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.苹果酸中能发生酯化反应的官能团有2种
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.1 mol苹果酸与足量金属Na反应生成1 mol H2
D.![]() 与苹果酸互为同分异构体
与苹果酸互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两个完全相同的装置,分别在它们的侧管中装入1.06g Na2CO3和0.84g NaHCO3 , 试管中各有10mL相同浓度的盐酸(如图),同时将两个侧管中的物质全部倒入各自的试管中,下列叙述正确的是( ) 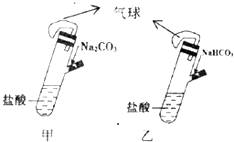
A.甲装置的气球膨胀速率大
B.若最终两气球体积相同,则一定有c(HCl)≥2 mol/L
C.若最终两气球体积不同,则一定有c(HCl)≤1 mol/L
D.最终两溶液中Na+、Cl﹣的物质的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com