
(1)最初混合气体中H2和N2的浓度。
(2)N2的转化率。
(3)若将N2的起始浓度改为6 mol·L-1,则达到平衡后NH3的浓度为4 mol·L-1,求平衡后N2和H2的转化率。
(1)最初N2的浓度为2.8 mol·L-1,氢气的浓度为6.5 mol·L-1
(2)N2的转化率为53.6%
(3)当N2起始浓度变化时,N2的转化率变为33.3%,H2的转化率为92.3%
解析:(1)设N2、H2的起始浓度为a、b。
N2 + 3H2![]() 2NH3
2NH3
起始浓度/mol·L
平衡浓度/mol·L-1 2.6/2 4.0/2 6.0/2
转化浓度/mol·L-1 1.5 4.5 3.0
根据计算式可知:[起始浓度]=[平衡浓度]+[转化浓度]
a=1.3+1.5=2.8(mol·L-1)
b=2.0+4.5=6.5(mol·L-1)
(2)N2转化率:![]() ×100%=53.6%
×100%=53.6%
(3)设N2、H2、NH3的转化浓度为?a′、b′、c′?。
N2+3H2![]() 2NH3
2NH3
起始浓度/mol·L-1 6 6.5 0
平衡浓度/mol·L-1 4.0
转化浓度/mol·L
根据化学方程式的比例可知c′=4.0 mol·L-1,
b′=6.0 mol·L-1,a′=2.0 mol·L-1
所以N2的转化率:![]() ×100%=33.3%
×100%=33.3%
H2的转化率:![]() ×100%=92.3%
×100%=92.3%


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
| 1 |
| 7 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
| 1 |
| 7 |
| ||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省南通市如皋市高三(上)期中化学试卷(解析版) 题型:填空题
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
 ,此时N2的转化率为 .
,此时N2的转化率为 . 4NO+6H2O 4NO+3O2+2H2O=4HNO3
4NO+6H2O 4NO+3O2+2H2O=4HNO3查看答案和解析>>
科目:高中化学 来源:0107 月考题 题型:不定项选择题
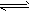
[ ]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com