
| A. | 水电离出的c(H+):②>① | |
| B. | c(NH4+):③>① | |
| C. | ①和②等体积混合后的溶液:c(H+)=c(OH- )+c(NH3•H2O) | |
| D. | ①和③等体积混合后显碱性,c(NH4+)>c(Cl-)>c(NH3•H2O ) |
分析 A.氨水和盐酸都抑制了是的电离,盐酸为强酸,抑制程度大于氨水;
B.一水合氨部分电离,氯化铵完全电离;
C.①和②等体积混合的溶液为氯化铵溶液,利用质子守恒来分析;
D.①和③等体积混合后的溶液氨水的电离大于氯化铵中铵根离子的水解.
解答 解:A.氨水和盐酸都抑制了是的电离,盐酸为强酸,抑制程度大于氨水,则盐酸中水电离出的氢离子浓度小于氨水,所以水电离出的c(H+):②>①,故A错误;
B.氯化铵为强电解质完全电离后产生大量的NH4+,氨水为弱电解质只有少量的NH4+产生,则c(NH4+)为③>①,故B正确;
C.盐酸和氨水混合后恰好完全反应,生成的盐为强酸弱碱盐,溶液显酸性,由质子守恒可知,c(H+)=c(OH-)+c(NH3•H2O),故C正确;
D.①和③等体积混合,溶液呈碱性,即氨水的电离大于氯化铵的水解,则c(NH+4)>c(Cl-)>c(NH3•H2O ),故D正确;
故选A.
点评 本题综合考查弱电解质的电离、盐类的水解以及离子浓度大小比较等相关知识,对于考生的要求较高,难度中等,注意把握溶液中离子浓度大小比较方法以及溶液中的守恒关系.


 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:解答题
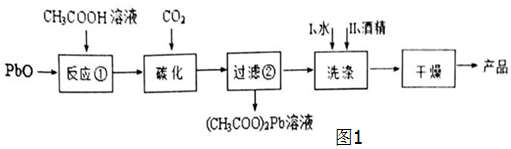
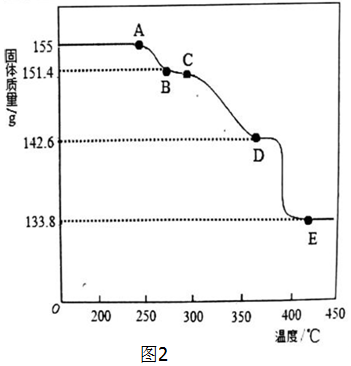
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | Cl2和NaCl中均含有氯元素,它们的化学性质相同 | |
| C. | 实验室制备Cl2可用排饱和食盐水集气法收集 | |
| D. | 氯气、液氯和氯水是一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分类是学习和研究化学物质及其变化的一种常用方法 | |
| B. | 有些液态胶体也是透明的,用肉眼很难与溶液相区别 | |
| C. | 2 L1 mol/L Na2 CO3溶液中c(Na+)为4 mol/L | |
| D. | 从1 LNaCl溶液中取出100 ml,其浓度与原1L溶液相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐的电离平衡被破坏 | B. | 溶液温度升高 | ||
| C. | 25℃,溶液的pH不是7 | D. | 水的电离平衡被破坏 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{m}{23V}$mol/L | B. | $\frac{23}{mV}$mol/L | C. | $\frac{2m}{23V}$mol/L | D. | $\frac{m}{46V}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物的熔点一定比共价化合物熔点高 | |
| B. | 甲烷的标准燃烧热为890.3KJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| C. | 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ•mol-1 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照条件和点燃条件下的△H相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com