
| A. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| B. | NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O | |
| C. | 硫化钠的水解反应:S2-+H3O+HS-+H2O | |
| D. | 将0.2 mol•L-1的NH4Al(SO4)2溶液与0.3 mol•L-1的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
分析 A.硝酸足量将二价铁离子氧化成三价铁离子;
B.氢氧化钡足量,碳酸根离子、铵根离子都反应;
C.硫离子水解生成硫氢根离子和氢氧根离子;
D.NH4Al(SO4)2与Ba(OH)2按照2:3物质的量之比反应生成氢氧化铝、硫酸钡和硫酸铵.
解答 解:A.Fe3O4溶于稀HNO3发生氧化还原反应生成硝酸铁、NO和水,离子方程式为3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,故A错误;
B.NH4HCO3溶液与足量Ba(OH)2溶液混合:NH4++HCO3-+Ba2++2OH-=BaCO3↓+H2O+NH3•H2O,故B错误;
C.硫化钠的水解反应,离子方程式:S2-+H2O=HS-+OH-,故C错误;
D.NH4Al(SO4)2与Ba(OH)2按照2:3物质的量之比反应生成氢氧化铝、硫酸钡和硫酸铵,离子方程式:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意反应物用量对反应的影响,注意硝酸的强氧化性,选项D为易错选项.;


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:选择题
| A. | 液态钠可用作核反应堆的传热介质 | |
| B. | 在过渡元素中寻找半导体材料 | |
| C. | 考古时利用l4C测定一些文物的年代 | |
| D. | 235U是一种重要核燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、H+、SO42-、OH- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、H+、Cl-、HCO32- | D. | Na+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
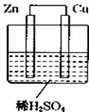 如图所示是 Zn 和 Cu 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( )
如图所示是 Zn 和 Cu 形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录卡如下,则卡片上的描述合理的是( )| A. | ②④⑤ | B. | ②③④⑤ | C. | ①④⑥ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
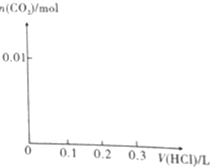 (1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.在如图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.
(1)将0.4gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.1mol•L-1稀盐酸.在如图所示坐标系中画出能正确表示加入盐酸的体积和生成CO2的物质的量的关系图象.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③②④⑤ | B. | ②①④⑤③ | C. | ②④①⑤③ | D. | ④⑤②①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据系统命名法,CH3-CH=CH-CHO的名称是:丁烯醛 | |
| B. | 1 mol HCHO发生银镜反应最多生成2 mol Ag | |
| C. | 对甲基苯甲醛( )使酸性高锰酸钾溶液褪色,说明它含有醛基 )使酸性高锰酸钾溶液褪色,说明它含有醛基 | |
| D. | 能发生银镜反应的有机物不一定是醛类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸中硫酸物质的量浓度为18.4 mol/L | |
| B. | 配制溶液所需浓硫酸体积为24mL | |
| C. | 配制溶液时仅需的仪器有容量瓶、烧杯、玻璃棒、量筒 | |
| D. | 配制溶液时,量取硫酸注入到烧杯中,加水稀释,冷却后再转移到容量瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com