
| ʵ��װ�� | ��� | ��ҺX | ʵ������ |
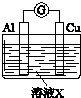 | ʵ��� | 6mol•L-1ϡ���� | ������ָ������ƫת��ͭƬ���������ɫ���壬��Һ���Ϸ���Ϊ����ɫ�� |
| ʵ��� | 15mol•L-1Ũ���� | ������ָ��������ƫת���ܿ���ƫ����ߣ���Ƭ��ͭƬ�����������ɫ���壬��Һ��Ϊ��ɫ�� |
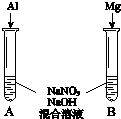 ��3������ͼװ�ý���ʵ�����ҺXΪ1mol•L-1ϡ������Һ���۲쵽������ָ������ƫת��
��3������ͼװ�ý���ʵ�����ҺXΪ1mol•L-1ϡ������Һ���۲쵽������ָ������ƫת������ ��1������ʵ�������֪��ʵ��1������ָ������ƫת��ͭƬ���������ɫ���壬��Һ���Ϸ���Ϊ����ɫ��˵����ԭ�������������������������Ӧ��ͭ�����������ᱻ��ԭ��һ���������ڿ����б������ɶ���������
��2��ʵ��2�е�����ָ��������ƫת���ܿ���ƫ����ߣ���Ƭ��ͭƬ�����������ɫ���壬��Һ��Ϊ��ɫ��˵����ʼ���Ǹ�����ͬʵ��1��ͭ�����ж��������������ܿ�����Ũ����ۻ���ͭ������������������Ӧ����������ͭ����Һ����ɫ��������ԭ�ɶ��������������缫�������ݴ˴��⣻
��3����ҺXΪ1mol•L-1ϡ������Һ����Ӧ�����Һ�к�NH4+��˵�����ᱻ��ԭ����笠����ӣ�ԭ���������������ͭ��������������������ԭ��笠����ӣ�
��4������������������Ӧ���������������л�ԭ�ԣ����Խ��������ԭ���ɰ��������ݵ���غ��Ԫ���غ��д�����ӷ���ʽ����þ���û�з�Ӧ��
��5��������������Һ�в�����������Ҳ�Ͳ��������Ʒ�Ӧ���ݴ˷�����
��� �⣺��1������ʵ�������֪��ʵ��1������ָ������ƫת��ͭƬ���������ɫ���壬��Һ���Ϸ���Ϊ����ɫ��˵����ԭ�������������������������Ӧ��ͭ�����������ᱻ��ԭ��һ���������ڿ����б������ɶ�����������Ӧ����ʽΪ2NO+O2=2NO2��
�ʴ�Ϊ������2NO+O2=2NO2��
��2��ʵ��2�е�����ָ��������ƫת���ܿ���ƫ����ߣ���Ƭ��ͭƬ�����������ɫ���壬��Һ��Ϊ��ɫ��˵����ʼ���Ǹ�����ͬʵ��1��ͭ�����ж��������������ܿ�����Ũ����ۻ���ͭ������������������Ӧ����������ͭ����Һ����ɫ��������ԭ�ɶ��������������缫������
�ʴ�Ϊ��Al��ʼ����صĸ�����Al��Ũ������Ѹ��������������Ĥ��Cu��������
��3����ҺXΪ1mol•L-1ϡ������Һ����Ӧ�����Һ�к�NH4+��˵�����ᱻ��ԭ����笠����ӣ�ԭ���������������ͭ��������������������ԭ��笠����ӣ�
��ʵ���Ҽ���NH4+�ķ����� ȡ����������Һ���Թ��У�����ŨNaOH��Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ���������壬����Һ�к�NH4+��
�ʴ�Ϊ��ȡ����������Һ���Թ��У�����ŨNaOH��Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ���������壬����Һ�к�NH4+��
������NH4+�ĵ缫��Ӧʽ��NO3-+8e-+10 H+=NH4++3H2O��
�ʴ�Ϊ��NO3-+8e-+10 H+=NH4++3H2O��
��4���ټ���������������Ӧ���������������л�ԭ�ԣ����Խ��������ԭ���ɰ��������ݵ���غ��Ԫ���غ��д�����ӷ���ʽ����þ���û�з�Ӧ��
�ʴ�Ϊ��Al��NaOH��Һ��Ӧ����H2�Ĺ����пɽ�NO3-��ԭΪNH3����Mg������NaOH��
�ڼ��������������������ԭ���ɰ�������Ӧ�����ӷ���ʽΪ8Al+3NO3-+5OH-+2H2O=3NH3��+8AlO2-��
�ʴ�Ϊ��8Al+3NO3-+5OH-+2H2O=3NH3��+8AlO2-��
��5��������������Һ�в�����������Ҳ�Ͳ��������Ʒ�Ӧ������������ ����
�ʴ�Ϊ����Ϊ�������Ե���������Һ������H2�Ĺ��̣�NO3-������ԭ��
���� ���⿼��ԭ��ع���ԭ������Ŀ�Ѷ��еȣ���ȷ��ͬŨ�ȵ����������ķ�Ӧ�ǽ����Ĺؼ�����ȷԭ��ص���������������Һ���������ʡ���һ�缫���ϵĻ��ǿ���йأ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
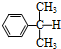 ���������ǹ�ҵ�������Ӻͱ�ͪ����Ҫ�ķ������䷴Ӧ���������£�
���������ǹ�ҵ�������Ӻͱ�ͪ����Ҫ�ķ������䷴Ӧ���������£�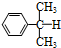 +O��
+O��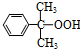 ������������⣩
������������⣩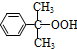 $��_{50-60��}^{H+}$
$��_{50-60��}^{H+}$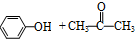 �����ã�
�����ã�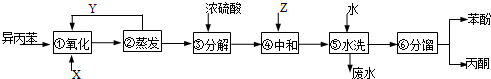
| ���� | ��ͪ | ���� | ����� |
| �ܶȣ�g/mL�� | 0.7898 | 1.0722 | 0.8640 |
| �е�/��C | 56.5 | 182 | 153 |
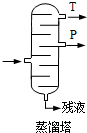 ����ƷT�DZ�ͪ��
����ƷT�DZ�ͪ�� ����1�����ᡢ�ڢڲ���KI��Һ��ҪѸ�ٸǺø��ӵ�ԭ�������ӷ���
����1�����ᡢ�ڢڲ���KI��Һ��ҪѸ�ٸǺø��ӵ�ԭ�������ӷ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
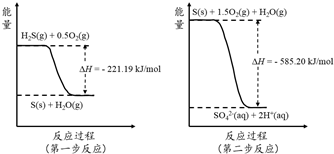
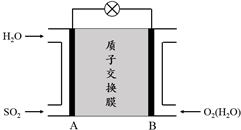
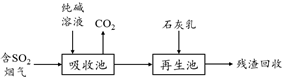
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��Һ�� Mg2+��Al3+��SO42-��CO32- | |
| B�� | pH=1����Һ�� NH4+��Ba2+��HCO3-��NO3- | |
| C�� | ��MnO4-����Һ�� H+��K+��Br-��I- | |
| D�� | ��$\frac{c��{H}^{+}��}{c��O{H}^{-}��}$=1��10-12����Һ�� Na+��K+��CH3COO-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O2+2H2O�T2Na++2OH-+H2�� | B�� | 2O22-+4H+�T4OH-+O2�� | ||
| C�� | Na2O2+2H2O�T2Na++2OH-+O2�� | D�� | 2Na2O2+2H2O�T4Na++4OH-+O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
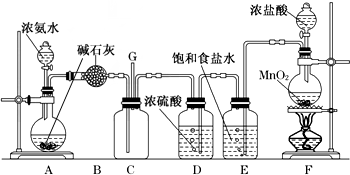
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
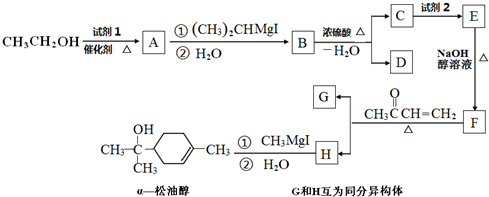
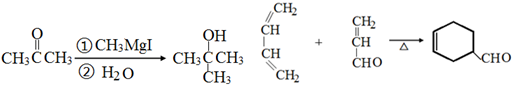
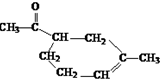 ��
��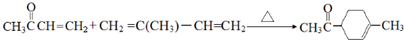 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 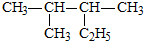 ������Ϊ2��3-�������� ������Ϊ2��3-�������� | |
| B�� | 18.0g��������������[CH3CH��OH��COOH]�������ȫȼ����������13.44L | |
| C�� | �ṹƬ��Ϊ �ĸ߾����ͨ���Ӿ۷�Ӧ���ɵ� �ĸ߾����ͨ���Ӿ۷�Ӧ���ɵ� | |
| D�� | ������ ������������Һ�м��Ⱥ���NH3���� ������������Һ�м��Ⱥ���NH3���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com