
| A£® | ĪŖ²ā¶ØČŪČŚĒāŃõ»ÆÄʵĵ¼µēŠŌ£¬½«ĒāŃõ»ÆÄĘ¹ĢĢå·ÅŌŚŹÆÓ¢ŪįŪöÖŠ¼ÓČČČŪ»Æ | |
| B£® | ½«Ņ»¶ØĮæµÄNa2O2ŗĶNaHCO3µÄ»ģŗĻĪļ·ÅŌŚŅ»ĆܱÕČŻĘ÷ÖŠ³ä·Ö¼ÓČČŗó£¬ĖłµĆ¹ĢĢåÖŠŅ»¶Øŗ¬ÓŠNa2CO3 | |
| C£® | ĮņĖį”¢“æ¼ī”¢Ę«ĀĮĖįÄĘŗĶ¹żŃõ»ÆÄĘ·Ö±šŹōÓŚĖį”¢¼ī”¢ŃĪŗĶŃõ»ÆĪļ | |
| D£® | ½«×ćĮæµÄĻ”ŃĪĖį¼Óµ½Mg”¢AlCl3”¢NaAlO2×é³ÉµÄ»ģŗĻĪļÖŠ£¬Ö»ÄÜ·¢ÉśŅ»ÖÖ·“Ó¦ |
·ÖĪö A£®¼ÓČČĢõ¼žĻĀ£¬ĒāŃõ»ÆÄĘŗĶ¶žŃõ»Æ¹č·“Ó¦£»
B£®Ģ¼ĖįĒāÄĘ¼ÓČČ·Ö½āÉś³É¶žŃõ»ÆĢ¼ŗĶĖ®£¬¶žŃõ»ÆĢ¼ĻČÓė¹żŃõ»ÆÄĘ·“Ó¦£»
C£®“æ¼īŹōÓŚŃĪ£»
D£®ŃĪĖįŗĶĆ¾”¢NaAlO2·“Ó¦£®
½ā“š ½ā£ŗA£®¼ÓČČĢõ¼žĻĀ£¬ĒāŃõ»ÆÄĘŗĶ¶žŃõ»Æ¹č·“Ó¦£¬æÉŹ¹ŪįŪöÕØĮŃ£¬¹ŹA“ķĪó£»
B£®Ģ¼ĖįĒāÄĘ¼ÓČČ·Ö½āÉś³É¶žŃõ»ÆĢ¼ŗĶĖ®£¬¶žŃõ»ÆĢ¼ĻČÓė¹żŃõ»ÆÄĘ·“Ӧɜ³ÉĢ¼ĖįÄĘ£¬¹ŹBÕżČ·£»
C£®“æ¼īĪŖĢ¼ĖįÄĘ£¬ŹōÓŚŃĪ£¬¹ŹC“ķĪó£»
D£®ŃĪĖįŗĶĆ¾”¢NaAlO2·“Ó¦£¬·Ö±šÉś³ÉĒāĘų”¢ĀČ»ÆĀĮ”¢ĀČ»ÆÄĘ£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŌŖĖŲ»ÆŗĻĪļÖŖŹ¶µÄ×ŪŗĻĄķ½āŗĶŌĖÓƵÄ漲飬עŅāĻą¹Ų»ł“”ÖŖŹ¶µÄ»żĄŪ£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

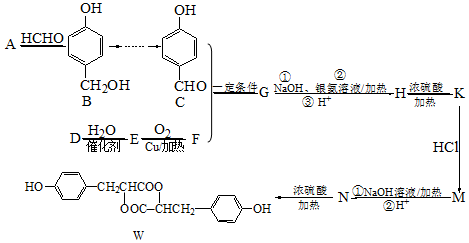
 £®
£®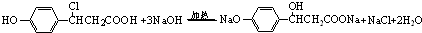 £®
£®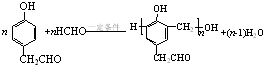 £®
£®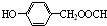 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2”¢SiO2”¢CO2¾łĪŖĖįŠŌŃõ»ÆĪļ | |
| B£® | Ļ”¶¹½¬”¢¹čĖį”¢ĀČ»ÆĢśČÜŅŗ¾łĪŖ½ŗĢå | |
| C£® | ÉÕ¼ī”¢±ł“×Ėį”¢ĖÄĀČ»ÆĢ¼”¢°±Ęų¾łĪŖµē½āÖŹ | |
| D£® | ø£¶ūĀķĮÖ”¢Ė®²£Į§”¢Ēā·śĖį”¢Š”ĖÕ“ņ¾łĪŖ“æ¾»Īļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
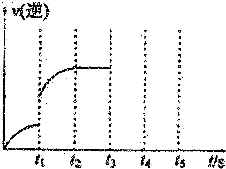 ¢ń£®Ģå»żĪŖ5LµÄŗćĪĀ”¢ŗćČŻĆܱÕČŻĘ÷¼×ĘšŹ¼Ķ¶Čė2molN2”¢3molH2¾¹żl0s“ļĘ½ŗā£¬²āµĆĘ½ŗāŹ±NH3µÄĪļÖŹµÄĮæĪŖ0.8mol£®
¢ń£®Ģå»żĪŖ5LµÄŗćĪĀ”¢ŗćČŻĆܱÕČŻĘ÷¼×ĘšŹ¼Ķ¶Čė2molN2”¢3molH2¾¹żl0s“ļĘ½ŗā£¬²āµĆĘ½ŗāŹ±NH3µÄĪļÖŹµÄĮæĪŖ0.8mol£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com