
三聚氰胺的结构简式如右:
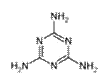 ⑴三聚氰胺的分子式为____________;分子中碳原子的杂化方式是______;分子中处于同一平面的氮原子有______个。
⑴三聚氰胺的分子式为____________;分子中碳原子的杂化方式是______;分子中处于同一平面的氮原子有______个。
⑵三聚氰胺的水溶液呈弱碱性,其原因是_______________________________________。
⑶三聚氰胺在高温下可释放氰化物,六氰合亚铁离子[Fe(CN)64-]中也含有CN-,写出一种与CN-互为等电子体的单质分子的路易斯结构式________________。
⑷三聚氰胺性状为纯白色单斜棱晶体,无味,密度1.573 g/cm3 (16 ℃)。常压熔点354 ℃(分解);快速加热升华,升华温度300 ℃。据此可判断三聚氰胺的晶体类型应为______________晶体。
⑸蛋白质的基本结构单元为氨基酸,其含氮量一般不超过30%,由于食品和饲料工业蛋白质含量测试方法的缺陷(以测定含氮量来确定蛋白质的含量),故三聚氰胺被不法分子用作食品添加剂,以提高食品检测中的蛋白质含量指标,故三聚氰胺被人称为“蛋白精”。通过计算说明三聚氰胺被称为蛋白精的理由。
⑴C3N6H6[C3N3(NH2)3];sp2杂化;6;⑵三聚氰胺溶于水可结合水分子中的氢原子而使溶液呈弱碱性。⑶![]() ;⑷分子;⑸三聚氰胺分子式为C3N6H6,其含氮量约为
;⑷分子;⑸三聚氰胺分子式为C3N6H6,其含氮量约为![]() =66.7%,远高于一般的蛋白质。
=66.7%,远高于一般的蛋白质。
解析:⑴从结构简式可以得出分子式为C3N6H6或[C3N3(NH2)3],由于三聚氰胺具有类似苯环的结构,其分子中碳原子的杂化方式应为sp2杂化方式,分子中处于同一平面的氮原子有6个。⑵三聚氰胺分子中含有三个氨基,溶于水可结合水分子中的氢原子而使溶液呈弱碱性。⑶CN-中共有14个电子,因此与它等电子体的单质为N2。⑷三聚氰胺熔点不高,易升化,故属分子晶体。⑸根据结构简式可知三聚氰胺分子式为C3N6H6,其含氮量约为66.7%,远高于一般蛋白质,掺入奶粉或其他食品中可提高食品的含氮量,从而造成蛋白质含量高的假象。


科目:高中化学 来源: 题型:
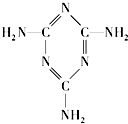 2008年9月份,国家质检总局查出多家知名品牌奶粉中含有三聚氰胺,长期饮用易导致肾结石.已知三聚氰胺的结构简式如图所示,下面对于其分类的说法正确的是( )
2008年9月份,国家质检总局查出多家知名品牌奶粉中含有三聚氰胺,长期饮用易导致肾结石.已知三聚氰胺的结构简式如图所示,下面对于其分类的说法正确的是( )查看答案和解析>>
科目:高中化学 来源:0103 月考题 题型:填空题

 则n值为_________。
则n值为_________。
查看答案和解析>>
科目:高中化学 来源:河北省期末题 题型:填空题

 ,则n值为_______。
,则n值为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
氮元素是生命活动、物质间转化的常见元素。
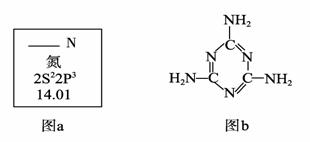
(1)图a是元素周期表中N元素的有关信息,图a中横线上缺失的具体内容是 。
15N是N元素的一种重要核素,其一个原子核中含有的中子数为 。
(2)三聚氰胺的结构简式如上图b,根据你的了解,下列关于三聚氰胺的表述中,
正确的是 (填字母序号)。
A.三聚氰胺的熔点可能很高 B.三聚氰胺的含氮量高达67%左右
C.三聚氰胺属于无机化合物 D.三聚氰胺分子中所有原子在同一平面上
(3)①最近科学家们合成了由氮元素形成的N5n+,电子式![]() 为
为
则n值为 。
②H与N能形成化合物NH5 ,已知该物质与水反应有H2生成,则NH5中含有的化学键为 。
(4)已知M为氮元素与一种金属元素组成的离子化合物,其中金属元素的质量分数为
35.4%,M在汽车安全气囊中有重要的作用。常温下G为淡黄色固体。H为一种常见的液体,A、B、C、X为单质,其中A、C、X为气体,A、X均为空气中成分。I、J为常见的工业原料。

①写出D与X反应的化学方程式
②写出G与H反应的离子方程式 。
③实验室中I应如何保存? 。
④常温下M受撞击时可分解,13gM完全分解为A和B时,放出akJ的热量,写出M分解的热化学方程式 。
⑤M是一种易溶于水的盐,其水溶液显弱碱性,用离子方程式解释原因 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com