
分析 (1)2A(g)+B(g)$\frac{\underline{\;\;△\;\;}}{\;}$ xC(g)+2D(s),
开始2 2 0 0
转化1.6 0.8
平衡0.4 1.2
以此计算转化率;
(2)2min时反应达到平衡状态,此时剩余1.2mol B,计算B的反应速率,反应速率之比等于化学计量数之比;
(3)利用平衡的特征“等、定”及由此衍生的物理量来判断平衡.
解答 解:(1)2A(g)+B(g)$\frac{\underline{\;\;△\;\;}}{\;}$ xC(g)+2D(s),
开始2 2 0 0
转化1.6 0.8
平衡0.4 1.2
则A的转化率为$\frac{1.6}{2.0}$×100%=80%,故答案为:80%;
(2)2min时反应达到平衡状态,此时剩余1.2mol B,则B的反应速率为$\frac{\frac{0.8mol}{2L}}{2min}$=0.2mol/(L.min),由反应速率之比等于化学计量数之比可知,x=3,
故答案为:3;
(3)2A(g)+B(g)$\frac{\underline{\;\;△\;\;}}{\;}$ 3C(g)+2D(s),
A.该反应中压强始终不变,不能判断平衡,故A错误;
B.因气体的质量在变化,则气体密度不再变化,达到平衡,故B正确;
C.因气体的质量在变化,则气体的平均相对分子质量不再变化,达到平衡,故C正确;
D.A的消耗速率与B的消耗速率之比为2:1,关系始终存在,不能判断平衡,故D错误;
故答案为:BC.
点评 本题考查化学平衡的计算、平衡的判定等,注意利用反应速率的关系确定x为解答的关键,注重高考常考考点的考查,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 热化学方程式中,如果没有注明温度和压强,则表示在标准状况下测得的数据 | |
| B. | 热化学方程式中,化学式前面的化学计量数既可表示微粒数,又可表示物质的量 | |
| C. | 书写热化学方程式时,不仅要写明反应热的符号和数值,还要注明各物质的聚集状态 | |
| D. | 凡是分解反应都是吸热反应,化合反应都是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
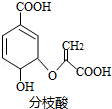
| A. | 可与乙醇、乙酸反应,且反应类型相同 | |
| B. | 分子中含有3种官能团 | |
| C. | 1mol分枝酸最多可与3molNaOH发生中和反应 | |
| D. | 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C2H4Cl2的物质一定是纯净物 | |
| B. | 分子组成符合CnH2n+2的烃一定是烷烃 | |
| C. | 正戊烷分子中所有碳原子均在一条直线上 | |
| D. | 碳氢原子个数比为1:3的烃有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2、SO2均是酸性氧化物,都能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与CO2反应产物也相同 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 二氧化硫有漂白性,通入少量紫色石蕊试液中,充分振荡后溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其氢氧化物中碱性最强的是NaOH | B. | 单质还原能力最强的是钠 | ||
| C. | 单质熔点最低的是钠 | D. | 原子半径逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
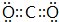 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 22.60 |
| 第二次 | 20.00 | 1.00 | 24.50 |
| 第三次 | 20.00 | 2.10 | 24.00 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com