
| A. | 可用澄清石灰水来区分二氧化碳和二氧化硫 | |
| B. | 用米汤检验食用加碘盐(含KIO3)中含有碘元素 | |
| C. | 能使灼热的CuO由黑变红的气体一定是H2 | |
| D. | 可用石蕊试液来鉴别盐酸和NaOH |
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题
| A. | MnO2与浓HCl作用:MnO2+4HCl(浓)$\stackrel{△}{→}$MnCl2+Cl2↑+2H2O | |
| B. | KMnO4+16HCl(浓)→2KCl+2MnCl2↑+5Cl2↑+8H2O | |
| C. | KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O | |
| D. | Ca(ClO)2+4HCl(浓)→CaCl2+2Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 解释 | |
| A | 100℃0.1mol/L Na2SO4溶液pH=6.2 | H2O=H++OH- |
| B | 0.1mol/L CH3COOH的pH=3 | CH3COOH?CH3COO-+H+ |
| C | 配制FeCl3溶液时加少量盐酸 | Fe3++3H2O?Fe(OH)3+3H+ |
| D | 随温度有升高,碳酸钠溶液pH增大 | CO32-+2H2O?H2CO3+2OH- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
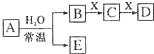 由短周期元素组成的中学常见无机物A、B、C、D、E、X 存在如在右图转化关系(部分生成物和反应条件略去),
由短周期元素组成的中学常见无机物A、B、C、D、E、X 存在如在右图转化关系(部分生成物和反应条件略去),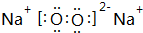 .将NaHCO3分解产生的气体(水蒸气和二氧化碳)用足量的A充分吸收得到固体甲,将甲溶于500mL 1mol/L的盐酸中,产生无色混合气体,溶液呈中性,则A的物质的量为0.25mol,混合气体在标准状况下的体积为2.8L(不考虑水蒸气的产生和其余气体的溶解).
.将NaHCO3分解产生的气体(水蒸气和二氧化碳)用足量的A充分吸收得到固体甲,将甲溶于500mL 1mol/L的盐酸中,产生无色混合气体,溶液呈中性,则A的物质的量为0.25mol,混合气体在标准状况下的体积为2.8L(不考虑水蒸气的产生和其余气体的溶解).查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应II 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
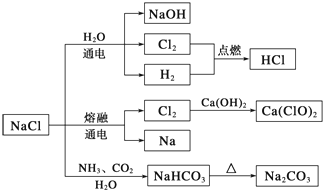
| A. | 25℃,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 电解NaCl溶液的阳极产物为H2和NaOH | |
| D. | 图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
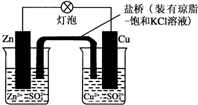
| A. | 负极反应为:Zn-2e-═Zn2+ | B. | 电池反应为:Zn+Cu2+═Zn2++Cu | ||
| C. | 在外电路中,电子从负极流向正极 | D. | 盐桥中的K+移向ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com