
| 实验事实 | 结论 | |
| ① | HCl的水溶液中存在H+和Cl- | HCl是离子化合物 |
| ② | NO2通入水中,发生反应,产物中有HNO3 | NO2是酸性氧化物 |
| ③ | 向FeCl3溶液中加入铜片,溶液逐渐变为蓝色 | 氧化性:Fe3+>Cu2+ |
| ④ | 等物质的量的Na和Al都完全反应,Al失电子多 | 金属性:Al>Na |
| ⑤ | 某无色溶液中加入氢氧化钠浓溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定有NH4+ |
| A. | ①② | B. | ①②④ | C. | ③⑤ | D. | ③④⑤ |
分析 ①氯化氢分子中不存在阴阳离子,属于共价化合物;
②酸性氧化物与水反应生成酸,而二氧化氮与水反应生成酸和NO;
③铜与铁离子发生氧化还原反应,证明了氧化性:Fe3+>Cu2+;
④金属性强弱与得失电子数的多少无关;
⑤某无色溶液中加入氢氧化钠浓溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,则溶液中一定含有铵根离子.
解答 解:①HCl分子中不存在阴阳离子,为共价化合物,溶于水后在水的作用下能够电离出氢离子和氯离子,在熔融状态下不导电,故①错误;
②NO2通入水中发生反应,产物中有HNO3和NO,而酸性氧化物与水反应只生成酸,所以二氧化氮不属于酸性氧化物,故②错误;
③向FeCl3溶液中加入铜片,溶液逐渐变为蓝色,说明铁离子将铜氧化成铁离子,证明了氧化性:Fe3+>Cu2+,故③正确;
④等物质的量的Na和Al都完全反应,Al失电子多,不能说明金属性Al的大于钠,钠失去电子能力大于铝,所以钠的金属性大于Al,故④错误;
⑤某无色溶液中加入氢氧化钠浓溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,生成的气体为氨气,证明溶液中一定含有NH4+,此方法为检验铵根离子的方法,故⑤正确;
根据分析可知,正确的为③⑤,
故选C.
点评 本题考查了常见离子的性质及检验方法,题目难度中等,明确常见离子的性质为巨大的根据,注意熟练掌握常见离子的经验方法,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:解答题

| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | 197 | 360 | 499 | X |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 营养平衡、合理用药是保证人体健康和生活质量的重要途径.
营养平衡、合理用药是保证人体健康和生活质量的重要途径.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为131 | B. | 质量数为53 | C. | 核外电子数为53 | D. | 中子数为131 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加酚酞显无色的溶液 | B. | 与Al 反应放出H2 的溶液 | ||
| C. | pH<7 的溶液 | D. | c(H+)>c(OH-)的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 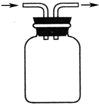 | C. |  | D. | 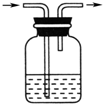 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com