
| A£® | ŹŹµ±¼ÓČČ | B£® | øÄÓĆŠæ·Ū | ||
| C£® | ¼ÓČėÉŁĮæNaClČÜŅŗ | D£® | ¼ÓČėÉŁĮæ1mol•L-1Ļ”ĮņĖį |
·ÖĪö øł¾ŻÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲ·ÖĪö£¬ČōŌö“ó·“Ó¦ĖŁĀŹ£¬æÉŅŌÉżøßĪĀ¶Č”¢Ōö“óŠæµÄ±ķĆ껿”¢Ōö“óĒāĄė×ÓÅØ¶ČµČ£¬¶ų¼ÓČėÉŁĮæĀČ»ÆÄĘČÜŅŗ£¬µ¼ÖĀŌČÜŅŗÖŠĒāĄė×ÓÅØ¶Č¼õŠ”£¬·“Ó¦ĖŁĀŹ¼õŠ”£¬¾Ż“Ė½ųŠŠ½ā“š£®
½ā“š ½ā£ŗA£®ŹŹµ±¼ÓČČ£¬»į¼Óæģ·“Ó¦ĖŁĀŹ£¬¹ŹA²»Ń”£»
B£®ŠæʬøÄĪŖŠæ·Ū£¬Ōö“óĮĖŠæµÄ½Ó“„Ć껿£¬æÉŅŌ¼Óæģ·“Ó¦ĖŁĀŹ£¬¹ŹB²»Ń”£»
C£®¼ÓČėÉŁĮæĀČ»ÆÄĘČÜŅŗ£¬ÄĘĄė×ÓŗĶĀČĄė×Ó²»ŠčŅŖŠæÓėĒāĄė×ӵķ“Ó¦£¬¶ųŌČÜŅŗÖŠĒāĄė×ÓÅØ¶Č¼õŠ”£¬µ¼ÖĀ·“Ó¦ĖŁĀŹ¼õŠ”£¬¹ŹCŃ”£»
D£®¼ÓČė1mol/LµÄĻ”ĮņĖį£¬Ōö“óĮĖČÜŅŗÖŠĒāĄė×ÓÅØ¶Č£¬“Ó¶ų¼ÓæģĮĖ·“Ó¦ĖŁĀŹ£¬¹ŹD²»Ń”£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ĖŁĀŹ¼°ĘäÓ°ĻģŅņĖŲ£¬ĢāÄæÄŃ¶Č²»“ó£¬Ć÷Č·Ó°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲĪŖ½ā“š¹Ų¼ü£¬ŹŌĢā²ąÖŲ»ł“”ÖŖŹ¶µÄæ¼²é£¬ÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeµÄĦ¶ūÖŹĮæĪŖ56g | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬71gCl2ŗ¬ÓŠNAøöCl2·Ö×Ó | |
| C£® | 1mol O2ŌŚ³£ĪĀĻĀµÄĢå»ż¶¼ĪŖ22.4L | |
| D£® | ½«1molNaCl¾§Ģå¼ÓČėµ½1LĖ®ÖŠ£¬µĆµ½NaClČÜŅŗµÄÅØ¶Č¾ĶŹĒ1mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČŻĘ÷ÄŚ${C_{£Ø{H_2}£©}}={C_{£Ø{I_2}£©}}={C_{£ØHI£©}}$ | B£® | ČŻĘ÷ÄŚµÄŃ¹Ēæ²»ŌŁ±ä»Æ | ||
| C£® | ¶ĻĮŃ1mol H-HµÄĶ¬Ź±Éś³É2mol H-I | D£® | ČŻĘ÷ÄŚŃÕÉ«²»ŌŁ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
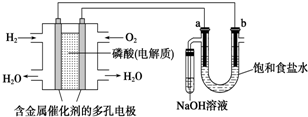
| A£® | µē³Ų¹¤×÷Ź±£¬Õż¼«·“Ó¦Ź½ĪŖ£ŗO2+2 H2O+4e-=4OH- | |
| B£® | ŗöĀŌÄÜĮæĖšŗÄ£¬µ±µē³ŲÖŠĻūŗÄ0.1g H2Ź±£¬b¼«ÖÜĪ§»į²śÉś1.12L H2 | |
| C£® | µē½āŹ±£¬µē×ÓĮ÷¶ÆĀ·¾¶ŹĒ£ŗøŗ¼«”śĶāµēĀ·”śŅõ¼«”śČÜŅŗ”śŃō¼«”śÕż¼« | |
| D£® | µē½āŹ±£¬a µē¼«ÖÜĪ§Ź×ĻČ·ÅµēµÄŹĒCl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šøÕŹÆŗĶŹÆÄ« | B£® | CH3CH2OHÓėCH3OCH3 | ||
| C£® | H2OŗĶD2O | D£® | ė®ŗĶė° |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¼×»łµÄµē×ÓŹ½£ŗ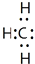 | B£® | 2-¶”Ļ©µÄ¼üĻߏ½£ŗ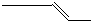 | ||
| C£® | ±ūĻ©µÄ½į¹¹¼ņŹ½£ŗCH2CHCH3 | D£® | ŅŅ“¼µÄ½į¹¹Ź½£ŗ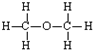 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4 L ±½ÖŠŗ¬ÓŠµÄ±½·Ö×ÓŹżŹĒNA | |
| B£® | ±ź×¼×“æöĻĀ£¬1molŗ¤ĘųÖŠŗ¬ÓŠµÄŗĖĶāµē×ÓŹżĪŖ2NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬15gŅŅĶé·Ö×ÓŹżÄæĪŖ NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬0.10 mol•L-1CH3COOHČÜŅŗÖŠŗ¬ÓŠµÄH+ŹżŠ”ÓŚ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
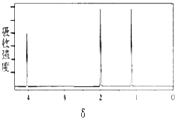
| A£® | CH3-CH2-CH3 | B£® | CH3CH2 CH2Br | C£® | 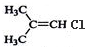 | D£® | 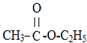 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com