
| A、酸性氧化物在一定条件下,都可以与碱反应生成盐和水 |
| B、一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物 |
| C、酸根离子中不可能含有金属元素 |
| D、还原产物只有还原性,氧化产物只有氧化性 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
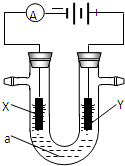 现有如下两个反应:
现有如下两个反应:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钠、纯碱以及水玻璃溶液要存放在带磨砂玻璃塞的试剂瓶中 |
| B、氢氟酸盛放在棕色玻璃试剂瓶中 |
| C、保存硫酸亚铁溶液时常在其中加颗铁钉 |
| D、金属钠保存在汽油中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、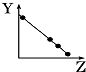 |
B、 |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有NaClO的溶液中:K+,NH4+,Fe3+,Br-,SO32- |
| B、所含溶质为Na2S2O3的溶液:K+、SO42-、NO3-、H+ |
| C、加入Mg能放出H2的溶液中:Mg2+,NH4+,Cl-,K+,SO42- |
| D、使甲基橙变红的溶液中:Fe2+,MnO4-,Na+,SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、随着原子序数的增加金属性增强 |
| B、碱金属的熔沸点从上至下增大 |
| C、碱金属元素与氧气反应的产物随着原子序数的增加而越复杂 |
| D、钾在水中的反应现象比钠剧烈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com