
| A. | 常见的周期表中,共有七个周期,三个短周期、四个长周期 | |
| B. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行 | |
| C. | 短周期元素,是指一、二、三周期,分别有2、8、8种元素 | |
| D. | ⅠA中的金属元素,称为碱金属元素,ⅦA元素又称为卤族元素 |
分析 元素周期表中有7个周期、7个主族,短周期为一、二、三周期,IA族含H元素及碱金属元素,以此来解答.
解答 解:A、共有三个短周期,4、5、6、7为四个长周期,故A正确;
B、元素周期表有16个族,7个主族、7个副族、1个0族、1个第ⅤⅢ族,其中第ⅤⅢ族占三个纵列,共18个纵行,故B错误;
C、一、二、三周期为短周期,分别有2、8、8种元素,故C正确;
D、第IA族的元素中除H元素外都是碱金属,第IA族的元素又称为碱金属元素,第VIIA族的元素都是非金属元素,又称为卤族元素,故D正确;
故选B.
点评 本题考查学生元素周期表的递变规律以及元素的分布知识,注意知识的归纳和整理是解题的关键,难度不大.


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a<b,则c<$\frac{1}{2}$(a+b) | B. | 若a<b,则c>$\frac{1}{2}$(a+b) | C. | 若a>b,则c=$\frac{1}{2}$(a+b) | D. | 若a=b,则c=$\frac{1}{2}$(a+b) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
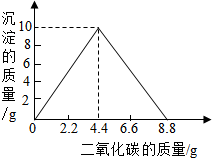 某实验小组在含一定量Ca(OH)2的澄清石灰水中通入CO2,产生沉淀的质量与通入CO2气体的质量的关系如图所示,回答下列问题:
某实验小组在含一定量Ca(OH)2的澄清石灰水中通入CO2,产生沉淀的质量与通入CO2气体的质量的关系如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属性A>B>D | |
| B. | B和C形成的化合物中可能有共价键 | |
| C. | 原子序数D>C>A>B | |
| D. | 四种元素中,最高价氧化物对应的水化物酸性最强的是B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法正确的是( )
用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法正确的是( )| A. | 阴极的电极反应式为:Cl-+2OH--2e -=ClO-+H2 O | |
| B. | 阳极的电极反应式为:2CN-+12OH--10e-=N2↑+2CO 32-+6H2O | |
| C. | 电解时使用锂钒氧化物二次电池(V2O5+xLi$?_{充电}^{放电}$LixV2O5)做电源,电池充电时a 电极的电极反应式为:LixV2O5_xe-=V2O5+xLi+ | |
| D. | 除去CN-的反应:2CN-+5ClO-+2H+=N2↑+2CO2↑+5Cl-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com