
【题目】按要求回答下列问题。
(1)磷酸钠(Na3PO4)在水溶液中的电离方程式为__ 。
(2)镁条在氮气中燃烧的化学方程式为___。
(3)过氧化钠与水反应的化学方程式为___。该反应中,氧化剂是___,还原剂是___。
(4)浓硫酸和碳在加热条件下反应的化学方程式为___。
科目:高中化学 来源: 题型:
【题目】现有42.4g由Fe、Al、Al2O3组成的混合物,将固体混合物分成两等份,将其中一份加入足量的NaOH溶液中充分反应后剩余固体质量为5.6g;将另一份完全溶解在600mL2mol/L的硫酸溶液中,收集到标准状况下的气体8.96 L,欲使该反应后溶液中的金属离子完全沉淀,至少应加入3mol/LNaOH溶液的体积是
A. 300mL B. 600mL C. 800mL D. 900mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究新的热点。 完成下列问题:
(1)CO2催化加氢合成CH3OCH3是一种CO2转化方法,其过程中主要发生下列反应:
反应I:![]()
反应Ⅱ:![]()
①写出CO和H2合成CH3OCH3的热化学方程式____。
②分别在2L恒温密闭容器甲(恒温恒容)、乙(恒温恒压)中,加入CO2和H2各1 mol的混合气体,假设只发生反应Ⅱ,则两容器中反应达平衡后放出或吸收的热量较多的是____(填“甲”或“乙”)。当反应5 min时,测得甲容器中压强变为原来的一半,则用CO2表示的反应的速率= ___。
③在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。其中:
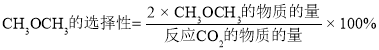
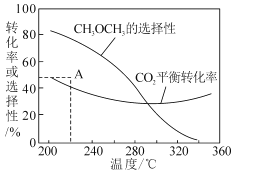
i)温度高于300℃,温度对CO2平衡转化率影响较大的是反应____(填“I”或“Ⅱ”)。
ii)220℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为48%(图中A点)。不改变反应时间和温度,一定能提高CH3OCH3选择性的措施可以是____(任答一条)。
(2)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为____(写离子符号);若所得溶液c(HCO3-):c(CO32-)=1:5,溶液pH= ___。(室温下,H2CO3的![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含ZnO、ZnS、CuS和SiO2及少量的Fe3O4。
I.某同学以该废催化剂为原料,回收其中的锌和铜。采用的实验方案如下:

回答下列问题:
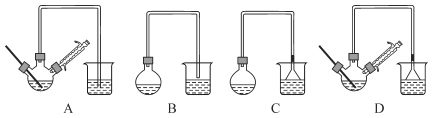
(1)在下图装置中,第一次浸出反应装置最合理的是____(填标号)。步骤①中发生的化学反应为非氧化还原反应,最好在(填设备名称)____中进行。
(2)滤液1中含有Fe2+,选用提供的试剂进行检验,检验方法为(提供的试剂:K3[Fe(CN)6]溶液、稀盐酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水)____。
(3)步骤③中发生反应的离子方程式为____;向盛有滤渣1的反应器中加入稀硫酸和过氧化氢溶液,应先加____,若顺序相反,会造成____。
(4)步骤②、④中,获得晶体的实验操作方法是____,过滤。
Ⅱ.另一同学也以该废催化剂为原料,采用下列实验操作方法也得到了ZnSO4。
![]()
(5)若一次水解时,产物为Zn( OH)xCly。取一次水解产物10. 64 g,经二次水解、干燥,得到9.9 g的Zn(OH)2(假设各步均转化完全),则一次水解产物的化学式为_______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. Fe2O3溶于过量氢碘酸溶液中:Fe2O3+6H++2I-===2Fe2++I2+3H2O
B. 0.1 mol·L-1 NH4Al(SO4)2溶液与0.2 mol·L-1 Ba(OH)2溶液等体积混合:Al3++2SO![]() +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO![]() +2H2O
+2H2O
C. 向0.1 mol·L-1、pH=1的NaHA溶液中加入NaOH溶液:HA-+OH-===A2-+H2O
D. 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O===HClO+HSO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
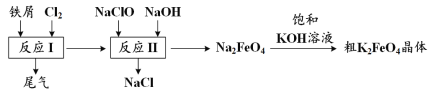
下列叙述不正确的是
A.用K2FeO4对饮用水杀菌消毒的同时,还产生Fe(OH)3胶体吸附杂质净化水
B.用FeCl2溶液吸收反应I中尾气后可再利用
C.反应II中氧化剂与还原剂的物质的量之比为3∶2
D.该生产条件下,物质的溶解性:Na2FeO4< K2FeO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法,正确的是( )
A.由甲烷在纯氧中完全燃烧只生成CO2和H2O说明甲烷不含氧元素
B.![]() 最多有16个原子共平面
最多有16个原子共平面
C.油脂在人体内水解为氨基酸和甘油等小分子才能被吸收
D.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用如图装置做以下两个实验:
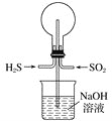
①常温下将H2S和SO2以物质的量之比为1∶1充满烧瓶,不久,烧瓶中能观察到的现象是_______。
②若用Cl2代替SO2,其他条件不变,观察到的现象与①相同之处为______,不同之处为_____;试用简要文字和化学方程式解释原因: ______。
③若想使②中反应后,烧瓶内产生“喷泉”现象,引发的操作为________。
(2)某课外活动小组利用如图所示装置进行实验:
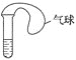
在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,因此溶液可能是_____溶液;加热时溶液由无色变为红色的原因是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离常数如下图中a、b两条曲线所示,曲线中的点都符合c(H+)×c(OH-)=常数。下列说法正确的是
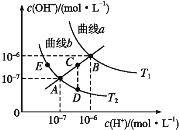
A. 图中温度T2>T1
B. 曲线a、b均代表纯水的电离情况
C. 图中五点的KW的关系:B>C>A>D=E
D. 若处在B点时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合后,溶液呈碱性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com