
【题目】下列气体可以用排水集气法收集的是
A. HCl B. SO2 C. NO D. NO2
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】2A(g) ![]() 2B(g) + C(g) △H < 0 ,现欲使正反应速率减小,C的浓度增大,可行的措施是(其它条件不变)( )
2B(g) + C(g) △H < 0 ,现欲使正反应速率减小,C的浓度增大,可行的措施是(其它条件不变)( )
A.加压 B.减压 C.减少C的浓度 D.降温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g)![]() H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为( )
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为( )
A. 25% B. 50% C. 75% D. 80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. SO2的漂白原理与次氯酸相同
B. 煤的干馏可得到石油气、汽油、煤油、柴油等
C. 从海水中提取所有物质都必须通过化学反应才能实现
D. 纯碱可用于生产普通玻璃,日常生活中也可用纯碱溶液来除去物品表面的油污
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家用氮化镓材料与铜组装成如图所示的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。下列关于该电池叙述错误的是( )
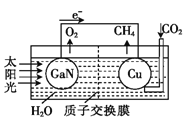
A.电池工作时,是将太阳能转化为电能
B. 铜电极为正极,电极反应式为:CO2+8e-+8H+=CH4+2H2O
C.电池内部H+透过质子交换膜从左向右移动
D.为提高该人工光合系统的工作效率,可向装置中加入少量硝酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、氮肥的使用在提高粮食产量的同时,也导致了土壤、水体污染等环境问题。
(1)长期过量使用铵态化肥NH4Cl,易导致土壤酸化,请用化学用语解释原因
(2)工业上处理氨氮废水的方法是采用电解法将NO3-转化为N2,如图所示


B极的电极反应方程式是_________________________
(3)除去60L废水中的62 mg NO3-后, 废水的pH= 。
Ⅱ、如下图所示C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色。
(1)若用甲醇、空气燃料电池作电源,电解质为KOH溶液,则A极的电极反应式为 。
(2)欲用(丙)装置给铜镀银,银应该是 电极(填G或H)。
(3)(丁)装置中Y极附近红褐色变 (填深或浅)。
(4)通电一段时间后,C、D、E、F电极均有单质生成,其物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成的,爆炸时的反应是:S+2KNO3+3C=K2S+N2↑+3CO2↑,该反应的还原剂是( )
A.C
B.C和S
C.KNO3
D.S和KNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。采用的实验方案如下:
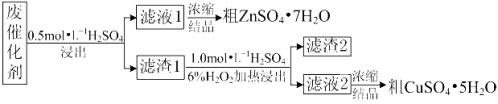
已知:① ZnS与稀硫酸反应时,化合价不变;
② CuS既不溶解于稀硫酸,也不与稀硫酸反应。
回答下列问题:
(1)在下列装置中,第一次浸出必须用________________,第二次浸出应选用______________。(填标号)。第二次浸出时,加热温度不宜过高的原因是 。

(2)滤液1中含有Fe2+,请根据提供的试剂进行检验,则检验方法为: 。
(提供的试剂:稀盐酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水)
(3)将滤液1、滤液2蒸发浓缩至 时,停止加热,然后冷却结晶得到相应的粗产品。
(4)若滤渣2中含有淡黄色固体,写出第二次浸出的化学反应方程式: 。
(5)某同学在实验完成之后,得到1.50 g CuSO4·5H2O,则铜的回收率为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com