
常温下,0.1mol/L某一元酸(HA)溶液中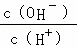 =1×10﹣8,下列叙述正确的是( )
=1×10﹣8,下列叙述正确的是( )
|
| A. | 溶液中水电离出的c(H+)=10﹣10mol/L |
|
| B. | 溶液中c(H+)+c(A﹣)=0.1 mol/L |
|
| C. | 溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH﹣)均增大 |
|
| D. | 与0.05mol/LNaOH溶液等体积混合后所得溶液中离子浓度大小关系为c(A﹣)>c(Na+)>c(OH﹣)>c(H+) |
考点:
弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
常温下Kw=c(OH﹣)×c(H+)=10﹣14,又知0.1mol/L某一元酸(HA)溶液中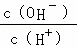 =1×10﹣8,解之得c(H+)=10﹣3mol/L,则HA为弱酸,以此解答该题.
=1×10﹣8,解之得c(H+)=10﹣3mol/L,则HA为弱酸,以此解答该题.
解答:
解:常温下Kw=c(OH﹣)×c(H+)=10﹣14,0.1mol/L某一元酸(HA)溶液中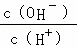 =1×10﹣8,得c(H+)=10﹣3mol/L,
=1×10﹣8,得c(H+)=10﹣3mol/L,
A.水电离出的c(H+)=c(OH﹣)= =
= mol/L=10﹣11mol/L,故A错误;
mol/L=10﹣11mol/L,故A错误;
B.溶液中c(H+)+c(A﹣)≈2c(H+)=2×10﹣3mol/L,故B错误;
C.溶液中加入一定量CH3COONa晶体,发生:CH3COO﹣+H+⇌CH3COOH,或加入水,都会导致c(H+)减小,c(OH﹣)增大,故C正确;
D.与0.05mol/LNaOH溶液等体积混合后,HA过量,则溶液应呈酸性,应有c(H+)>c(OH﹣),故D错误.
故选C.
点评:
本题考查弱电解质的电离,题目难度不大,本题注意根据溶液中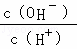 =1×10﹣8结合Kw计算溶液中c(H+)为解答该题的关键.
=1×10﹣8结合Kw计算溶液中c(H+)为解答该题的关键.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
化学已经渗透到人类生活的各个方面,下列说法不正确的是()
A. 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能消毒杀菌又能净水
B. 我国神九三位宇航员所穿航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
C. 多用电子邮件、MSN、QQ等即时通讯工具,少用传真打印机属于“低碳生活”方式
D. 高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路”
查看答案和解析>>
科目:高中化学 来源: 题型:
用标准氢氧化钠溶液中和醋酸溶液,当溶液的pH值等于7,则此时( )
|
| A. | 醋酸和氢氧化钠物质的量相等 |
|
| B. | 醋酸和氢氧化钠恰好中和 |
|
| C. | 氢氧化钠过量 |
|
| D. | 醋酸有剩余 |
查看答案和解析>>
科目:高中化学 来源: 题型:
含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为Va、Vb,则两者的关系正确的是( )
|
| A. | Va>10Vb | B. | Va=10Vb | C. | Vb<10Va | D. | Vb>10Va |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子:(1)I﹣、Fe2+、NO3﹣、H+(2)K+、NH4+、HCO3﹣、OH﹣ (3)SO32﹣、SO42﹣、K+、OH﹣(4)Fe2+、Cu2+、SO42﹣、Cl﹣ (5)Fe3+、SCN﹣、K+、SO42﹣ (6)H+、K+、AlO2﹣、HSO3﹣ 在溶液中能大量共存且溶液为无色的组别共有( )
|
| A. | 1组 | B. | 2组 | C. | 3组 | D. | 不少于4组 |
查看答案和解析>>
科目:高中化学 来源: 题型:
以下框图中A~M是中学化学常见的物质,其中A、E是金属,F和J为气体单质,其余均为化合物或其溶液,C为淡黄色固体,D为红棕色粉末,M为红褐色固体.
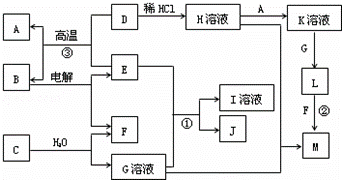
(1)B的化学式 ;
(2)19.5gC与足量的水反应转移电子的物质的量为 mol;
(3)写出物质C的电子式 ;
(4)写出②、③反应的方程式② ,③ .
查看答案和解析>>
科目:高中化学 来源: 题型:
以NA表示阿伏伽德罗常数,下列说法正确的是()
A. 0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA
B. 0.1mol Na2SO4溶液中,含有SO42﹣数为0.1NA
C. 46gNO2和N2O4混合气体中,含有氧原子总数为3NA
D. 0.5L 1mol/LNaCl溶液中含有的钠离子浓度1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com