
 4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 ;
4.7×10-8。写出向“84消毒液”(主要成分为氯化钠和次氯酸钠)中通入二氧化碳发生反应的离子方程式 ;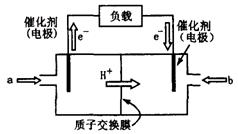
 意图。电池总反应为2CH3OH+3O2
意图。电池总反应为2CH3OH+3O2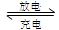 2CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为 ;
2CO2+4H2O。该装置放电时 (填“a”或“b”)为电池的负极,其电极反应式为 ;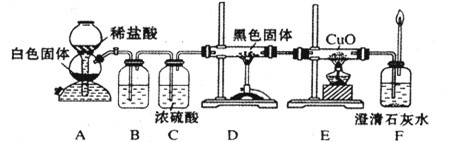
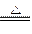 CO+H2 CO + H2O
CO+H2 CO + H2O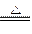 CO2 +
CO2 +  H2 C + CO2
H2 C + CO2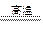 2CO
2CO 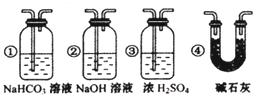
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源:不详 题型:填空题

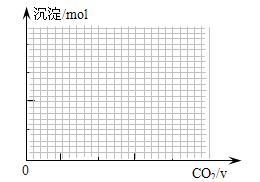
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硅氧键比氢氧键强,所以,二氧化硅的熔点高于冰的熔点 |
| B.1mol SiO2含有4mol Si—O键 |
C.粗硅精炼原理:SiO2+2C Si+2CO↑ Si+2CO↑ |
| D.二氧化硅溶于水生成硅胶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,甲溶液中溶质的物质的量浓度为 ,乙溶液中溶质的物质的量浓度为 。
,甲溶液中溶质的物质的量浓度为 ,乙溶液中溶质的物质的量浓度为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.青石棉是一种硅酸盐产品 |
| B.青石棉的化学组成用氧化物的形式可表示为:Na2O·3FeO ·Fe2O3·8SiO2·H2O |
| C.青石棉中含有一定量的石英晶体 |
| D.1mol 青石棉能使1mol硝酸被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.单质硅具有良好的导电性能 |
| B.光导纤维的主要成份是二氧化硅 |
| C.二氧化硅是H2SiO3的酸酐,因此能与水反应,也能与碱溶液反应 |
| D.硅酸盐是由二氧化硅与金属氧化物组成的混合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
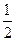 H2(g)+
H2(g)+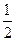 Cl2(g)==HCl(g) △H=—92.3kJ/mol
Cl2(g)==HCl(g) △H=—92.3kJ/mol
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B.水玻璃可用于生产黏合剂和防火剂 | C.二氧化硅广泛用于制作光导纤维 |
| D.北京奥运会“金镶玉” 奖牌玉的化学成分为含水钙镁硅酸盐。如Ca2Mg5Si8O22(OH)2可用氧化物表示为2CaO.5MgO.8SiO2.H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com