
下列各装置中,在铜电极上不能产生气泡的是

科目:高中化学 来源:2014-2015学年内蒙古巴市高一10月月考化学试卷(解析版) 题型:选择题
下列有关过滤实验的操作中不正确的是
A.过滤操作中,玻璃棒与三层滤纸相互接触
B.过滤操作中,漏斗颈与烧杯内壁相互接触
C.过滤操作中,玻璃棒与烧杯口相互接触
D.为加快过滤,使用玻璃棒搅动漏斗里的液体
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高二上学期期中化学试卷(解析版) 题型:实验题
(16分)为探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:

将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5 min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应.
(1)装置I中①的化学方程式为______________ __________________________,
_____________ ____________________________.
②中离子方程式为__________________________________________________.
(2)①中长导管的作用是________________________________________________.
(3)烧瓶中生成的红褐色油状液滴的成分是__________________________,要想得到纯净的产物,可用_____________________试剂洗涤.洗涤后分离粗产品应使用的仪器是____________________.
(4)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验.可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳.
a的作用是__________________________________________________________.
b中的试剂是__________________________________________________________.
比较两套装置,装置Ⅱ的主要优点是_______________________________.
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高二上学期期中化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.乙醇能发生氧化反应而乙酸不能发生氧化反应
B.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应
C.乙烯、聚氯乙烯都能使溴水褪色
D.苯、乙醇、乙酸都能发生取代反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三上学期第四次月考化学试卷(解析版) 题型:填空题
(12分)工业上金属的冶炼过程复杂。
(1)炼铁涉及的2个热化学方程式:
Fe2O2(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) △H=-15.73kJ?mol-1
Fe3O4+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ?mol-1
则反应Fe2O3(s)+CO(g)=2FeO(s)+CO2(g)的△H=__________;
(2)工业上电解硫酸锌溶液可实现湿法炼锌(控制条件,使H+难放电、阳极电极不溶解).写出电解总反应离子方程式____________________;
(3)将干净的铁片浸于熔融的液态锌水中可制得镀锌钢板,这种钢板具有很强的耐腐蚀能力。镀锌钢板的镀层一旦被破坏后,锌将作为原电池的___极发生___反应。(填“氧化”或“还原”)
(4)实验室用镀锌钢板与稀硫酸制取标准状况下的氢气4.48L,则该反应转移的电子数为______,消耗硫酸的物质的量是_____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三上学期第四次月考化学试卷(解析版) 题型:选择题
密闭容器中,有可逆反应Z(g)+W(g) X(?)+2Y(?)发生,Z的转化率随温度和压强变化关系如图所示,有关该平衡体系的说法不正确的是
X(?)+2Y(?)发生,Z的转化率随温度和压强变化关系如图所示,有关该平衡体系的说法不正确的是
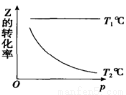
A.T1℃温度下发生反应的平衡常数表达式为K=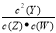
B.T1℃温度下混合气体的平均相对分子质量保存不变时,反应达到平衡
C.升高温度至T2℃,平衡常数K减小
D.增加X的量,平衡一定逆向移动
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三上学期第四次月考化学试卷(解析版) 题型:选择题
已知25℃、101kPa时,1g甲醇(CH3OH)完全燃烧生成CO2和液态H2O,同时发出22.68kJ热量。则下列表示该反应的热化学方程式正确的是
A.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(g) △H=-725.8kJ?mol-1
B.2 CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1451.6kJ
C.2 CH3OH+3O2=2CO2+4H2O △H=-22.68kJ?mol-1
D.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ?mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省东台市高二12月月考化学试卷(解析版) 题型:选择题
化学反应的实质就是旧键的断裂和新键的形成。欲探讨发生化学反应时分子中化学键在何处断裂的问题,近代科技常用同位素示踪原子法。如有下列反应:

可以推知,物质 发生此反应时断裂的化学键应是
发生此反应时断裂的化学键应是
A.①③ B.①④ C.② D.②③
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省伊春市高一上学期期中化学试卷(解析版) 题型:选择题
某工厂排放的工业废水中可能含有K+、H+、Mg2+、SO42-、Cl-、NO3-等离子。经检测废水呈明 显的碱性,则可确定该厂废水中肯定不含有的离子组合是
A.H+、Mg2+ B.K+、NO3-、SO42-
C.H+、K+、NO3- D.K+、Mg2+、SO42-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com