
如图所示实验装置、试剂选用或操作正确的是( )
|
| A. |
除去NO中的NO2 | B. |
铁制品表面镀锌 | C. |
稀释浓硫酸 | D. |
制取少量氨气 |
| 化学实验方案的评价;电解原理;氨的实验室制法;气体的净化和干燥;配制一定物质的量浓度的溶液.. | |
| 专题: | 实验评价题. |
| 分析: | A.二氧化氮和水反应生成硝酸和一氧化氮; B.应用硫酸锌溶液; C.容量瓶不能稀释溶液; D.氯化铵受热易分解,氨气和氯化氢又生成氯化铵. |
| 解答: | 解:A.二氧化氮能和水反应生成一氧化氮,可除掉杂质,故A正确; B.铁制品表面镀锌,锌作阳极,电解质溶液应该为硫酸锌,故B错误; C.容量瓶不能稀释溶液或溶解固体,只能配制溶液,故C错误; D.加热条件下,氯化铵分解生成氨气和氯化氢,温度较低时,氯化氢和氨气能立即反应生成氯化铵,故D错误. 故选A. |
| 点评: | 本题考查了气体的制取、洗气装置、溶液的配制、电解等知识点,难度不大,注意根据物质的性质选取合适的装置. |


科目:高中化学 来源: 题型:
图中,“——”表示相连的物质间在一定条件下可以反应,“—→”表示丁在一定条件下可以转化为乙。下面四组选项中,符合图示要求的是( )
| 甲 | 乙 | 丙 | 丁 | |
| A | H2SO4 | Na2SO4 | NaOH | NaCl |
| B | KCl | K2CO3 | KOH | HCl |
| C | O2 | CO | CuO | C |
| D | Fe | CuCl2 | Ag | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是( )
|
| A. | 元素原子最外层电子数的多少是判断金属性和非金属性强弱的依据 |
|
| B. | OH﹣与H3O+组成元素相同,所含质子数相同 |
|
| C. | 结构示意图为 |
|
| D. | H、D、T具有相同的质子数,是氢元素的三种同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为部分短周期元素化合价及其相应原子半径的数据.请回答下列问题:
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 原子半径(nm) | 0.102 | 0.117 | 0.074 | 0.110 | 0.071 | 0.075 | 0.077 | 0.099 |
| 最高化合价 | +6 | +4 | +5 | +5 | +4 | +7 | ||
| 最低化合价 | ﹣2 | ﹣4 | ﹣2 | ﹣3 | ﹣1 | ﹣3 | ﹣4 | ﹣1 |
(1)元素G在周期中的位置是 ;元素F所形成的常见单质的电子式为 .
(2)A、B、C、E的简单氢化物稳定性顺序是 (用化学式回答).
(3)分子组成为ACH2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸.该反应的化学方程式是 .
(4)请写出B的单质的一种重要用途: ;工业上制取该单质的原理反应为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
|
| A. | 1.0mol•L﹣1的KNO3溶液:H+、Fe2+、Cl﹣、SO42﹣ |
|
| B. | 甲基橙呈红色的溶液:NH4+、Ba2+、AlO2﹣、Cl﹣ |
|
| C. | c(H+)=10﹣12mol•L﹣1的溶液:K+、Ba2+、Cl﹣、Br﹣ |
|
| D. | 加入苯酚显紫色的溶液:K+、NH4+、Cl﹣、I﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应N2(g)+3H2(g)⇌2NH3(g)+Q;Q>0,下列研究目的和示意图相符的是 ( )
| A | B | C | D | |
| 研究目的 | 压强对反应的影响(P2>P1) | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 |
|
|
|
|
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列正确的叙述有( )
①CO2、NO2、P2O5均为酸性氧化物
②Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得
③碘晶体分散到酒精中、饱和氯化铁溶液滴入沸水中所形成的分散系分别为:溶液、胶体
④灼热的炭与CO2的反应、Ba(OH)2•8H2O与NH4Cl的反应均既为氧化还原反应,又是吸热反应
⑤需要通电才可进行的有:电离、电解、电镀、电化学腐蚀
⑥氯化铝溶液与氢氧化铝胶体具有的共同性质是:能透过滤纸,加热蒸干、灼烧后都有氧化铝生成
⑦苛性钾、次氯酸、氯气按顺序分类依次为:强电解质、弱电解质和非电解质
⑧金属元素和非金属元素形成的化合物一定是离子化合物.
|
| A. | 3个 | B. | 4个 | C. | 5个 | D. | 6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2•yCuCO3.
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2•CuCO3.某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50mol•L﹣1的Cu(NO3)2溶液、2.0mL 0.50mol•L﹣1的NaOH溶液和0.25mol•L﹣1的Na2CO3溶液按表Ⅰ所示体积混合.
实验2:将合适比例的混合物在表Ⅱ所示温度下反应.
实验记录如下:
| 编号 | V (Na2CO3)/mL | 沉淀情况 | 编号 | 反应温度/℃ | 沉淀情况 | |
| 1 | 2.8 | 多、蓝色 | 1 | 40 | 多、蓝色 | |
| 2 | 2.4 | 多、蓝色 | 2 | 60 | 少、浅绿色 | |
| 3 | 2.0 | 较多、绿色 | 3 | 75 | 较多、绿色 | |
| 4 | 1.6 | 较少、绿色 | 4 | 80 | 较多、绿色(少量褐色) |
表Ⅰ表Ⅱ
①实验室制取少许孔雀石,应该采用的条件是 n[Cu(NO3)2]:n(Na2CO3)=2:1,75℃ .
②80℃时,所制得的孔雀石有少量褐色物质的原因是 Cu(OH)2受热分解为CuO .
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:
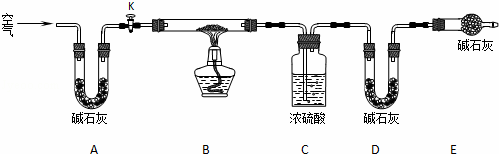
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4: 继续通一段时间空气至装置冷却 .
步骤5:称量相关装置的质量.
①装置A的作用是 除去空气中的CO2和H2O ;若无装置E,则实验测定的x/y的值将 偏小 (选填“偏大”、“偏小”或“无影响”).
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定x/y的值,你认为可以选用上述所采集数据中的 BC、BD、CD (写出所有组合的字母代号)一组即可进行计算,并根据你的计算结果,写出该样品组成的化学式 5Cu(OH)2•2CuCO3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关溶液组成的描述合理的是
A.无色溶液中可能大量存在Al3+、NH4+、Cl‾、S2‾
B.酸性溶液中可能大量存在Na+、ClO‾、SO42‾、I‾
C.弱碱性溶液中可能大量存在Na+、K+、Cl‾、HCO3‾
D.中性溶液中可能大量存在Fe3+、K+、Cl‾、SO42‾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com