
14分)
(一)下列有关实验操作或判断不正确的是 (填序号)。
A.配制一定物质的量浓度溶液,定容时平视刻度线。
B.苯、四氯化碳、乙醇三种有机溶剂都可用来萃取溴水中的溴。
C.让一束光通过胶体,从垂直于光线的方向可以看到一条光亮的“通路”。
D.配制100mL1mol/L的NaOH溶液,需称量4g的氢氧化钠固体。
E.用铂丝蘸取少量溶液做焰色反应,没有观察到紫色,所以该溶液中不含钾元素。
(二)实验室需要480mL0.1mol/LNa2CO3溶液,现用碳酸钠晶体配制,回答下列问题:
(1)应用托盘天平称取十水合碳酸钠(Na2CO3·10H2O)晶体 g。
(2)本实验还需要的仪器有 。
(3)若实验遇下列情况,溶液的浓度将会(填偏高、偏低、不变)
A.加水定容时俯视刻度线 ;
B.容量瓶内壁附有水珠而未干燥处理 ;
C.称量的碳酸钠晶体部分失结晶水 ;
(4)请你帮助把标签上的内容写一下(如图)。
(一)B D E (填序号)。 (二)(1) 14.3g。 (2) 烧杯、玻璃棒、500mL容量瓶、胶头滴管。
(3) A、偏高 B、不变 C、偏高 (4)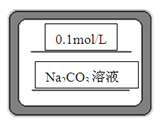
解析试题分析:(一)A、配制一定物质的量浓度溶液,定容时平视凹液面最低处刻度线,如果俯视容量瓶中溶液体积偏小,则配制的溶液浓度偏大。仰视正好相反,浓度偏小,A正确;B、乙醇和水能互溶,不能用作萃取剂,B错误;C、胶体具有丁达尔效应,所以让一束光通过胶体,从垂直于光线的方向可以看到一条光亮的“通路”,C正确;D、托盘天平读数到0.1g,所以需要称量NaOH固体的质量m=cVM=1mol/L×0.1L×40g/mol=4.0g,D错误;E、K元素的焰色反应需要透过蓝色钴玻璃观察,以滤去黄光的干扰,因此用铂丝蘸取少量溶液做焰色反应,如果没有观察到紫色,不能确定该溶液中不含钾元素E错误,答案选BDE。
(二)(1)由于实验室没有480ml的容量瓶,因此要配制48ml的溶液,需要选择500ml容量瓶。因此Na2CO3的物质的量n=cV=0.5L×0.1mol?L-1=0.05mol,Na2CO3?10H2O的物质的量等于Na2CO3的物质的量,所以Na2CO3?10H2O的质量0.05mol×286g/mol=14.3g;
(2)配制一定物质的量浓度如的基本操作步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等。一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,因此需要的仪器为托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管;
(3)根据c=n÷V可知,A、加水定容时俯视刻度线,则溶液体积偏小,所配溶液浓度偏高;B、容量瓶内壁附有水珠而未干燥处理,溶液的体积不变,所配溶液浓度不变;C、称量的碳酸钠晶体部分失水,溶质的质量偏大,所配溶液浓度偏高;
(4)标签上的内容为Na2CO3溶液,0.1mol/L。
考点:考查化学实验方案设计与评价;一定物质的量浓度溶液的配制


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:单选题
材料科学、能源科学、信息科学是二十一世纪的三大支柱产业。在信息通信方面,能同时传输大量信息,且具有较强抗干扰能力的材料是
| A.光导纤维 | B.塑料 | C.橡胶 | D.纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学与环境、材料、信息、能关系密切,下列说法正确的是
| A.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| B.绿色化学的核心是利用化学原理治理环境污染 |
| C.将煤气化或液化,获得清洁燃料 |
| D.PM2.5是指大气中直径接近于2.5×10-6 m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成混合物具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(1分)实验室要用98%(密度为1.84 g·cm-3)的硫酸配制3.68 mol/L的硫酸500 mL。
若配制3.68 mol/L的硫酸,其他操作均正确,下列操作会使所配硫酸溶液浓度偏低的是___。
| A.将稀释的硫酸转移至容量瓶后,未洗涤烧杯和玻璃棒 |
| B.将烧杯内的稀硫酸向容量瓶内转移时,因操作不当使部分稀硫酸溅出瓶外 |
| C.用胶头滴管向容量瓶中加水时凹液面高于容量瓶刻度线,此时立即用胶头滴管将瓶内多余液体吸出,使溶液凹液面与刻度线相切 |
| D.用胶头滴管向容量瓶中加入水时,仰视观察溶液凹液面与容量瓶刻度线相切 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
8分)准确称取12 g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100 mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol·L-1的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:
请填空回答:
(1)H2SO4溶液的物质的量浓度为_________________。
(2)若a=4.6,用于沉淀Fe3+消耗NaOH的体积是____________mL,铝土矿中各成分的质量分数:Al2O3为______________, SiO2为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(14分)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4 +16HCl(浓) 2KCl + 2MnCl2 + 5Cl2↑ +8H2O
(1)用单线桥法标出电子转移的方向和数目。
(2)该反应中的氧化剂与还原剂物质的量之比是 。
(3)KMnO4的氧化性比Cl2的氧化性 (选填“强”或“弱”)。
(4)如反应中转移了2mol电子,则产生的Cl2在标准状况下体积为 L。
(5)某同学欲用KMnO4固体配制100 mL0.5mol.L-1的溶液。回答下列问题:
①配制KMnO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、 、 。
②应用托盘天平称取KMnO4固体 g。
③不规范的实验操作会导致实验结果的误差。分析下列操作对实验结果的影响偏小的是(请填序号) 。
| A.加水定容时俯视刻度线 |
| B.容量瓶内壁附有水珠而未干燥处理 |
| C.颠倒摇匀后发现凹液面低于刻度线又加水补上 |
| D.在溶解过程中有少量液体溅出烧杯外 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(7分)暗紫色化合物A可作为电极材料的新型超铁电磁,因具有绿色、高电压和高能量的特点,近年来引起了电化学界的高度重视。在常温和干燥的条件下,化合物A可以稳定的存在,但它在水溶液中不稳定,一段时间后转化为红褐色沉淀。为探究其成分,某学习兴趣小组的同学取化合物A粉末进行试验。经组成分析,该粉末仅含有O、K、Fe三种元素。另取3.96g化合物A的粉末溶于水,滴加足量的稀硫酸,向反应后的溶液中加入含有0.08mol KOH的溶液,恰好完全反应。过滤,将洗涤后的沉淀充分灼烧,得到红棕色固体粉末1.60g;将所得滤液在一定条件下蒸发可得到一种纯净的不含结晶水的盐10.44g。
(1)3.96 g化合物A中含有Fe元素的物质的量为 mol,含有钾元素的物质的量为 mol。化合物A的化学式为 ;
(2)化合物A与H2O反应的离子方程式为 。
(3)为研究温度对化合物A水溶液稳定性的影响,请设计一个实验方案 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com